

图15-25
A.加热NaHCO3制CO2?
B.用Cu与稀HNO3反应制NO?
C.用NH4Cl与浓NaOH溶液反应制NH3?
D.用Zn与稀H2SO4反应制H2?
科目:高中化学 来源:江苏省通州市石港中学2008届高三化学科预测卷 题型:058
实验化学:
2005年江苏酸雨污染有所加重,酸雨发生频率为34.1%,上升了6.2个百分点,每三场雨中就有一场多是酸雨.某校研究性学习小组拟对本市空气中二氧化硫含量(mg·m-3)进行测定.经查阅资料可用以下方法测定:
实验原理:大气中的二氧化硫用甲醛溶液吸收后,生成稳定的羟甲基磺酸加成化合物,再加入氢氧化钠使加成化合物分解,释放出二氧化硫与副玫瑰苯胺、甲醛作用,生成紫红色化合物.据其颜色深浅,用分光光度计在577 nm处进行测定.
分光光度计是利用分光光度法对物质进行定量定性分析的仪器.而分光光度法则是通过测定被测物质在特定波长时光的吸收度,对该物质进行定性和定量分析.其工作原理可以简单的用公式表示为A=KC,其中A为吸光度,K为一定条件下的常数,C为溶液浓度.
实验步骤:(1)采样:
①如果你是该兴趣小组成员,你对采样的地点和时间有何建议:
___________________________________
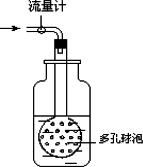
②用如图装置采样,通过50 L空气后,将吸收液移入100 ml容量瓶,用少量吸收液分两次洗涤吸收装置,合并洗涤液于容量瓶中,定容备用.
用多孔球泡而不用导管的原因是____________________________.
(2)吸光度与SO2含量标准曲线的绘制:在6支25 ml比色管中,用每毫升含25 μg二氧化硫的标准液配置下表标准SO2含量系列.
二氧化硫标准系列

用10 mL比色皿,以水为参比,测定各管吸光度,实验结果如下.

以吸光度值为纵坐标,二氧化硫含量(μg/10 mL)为横坐标,绘制标准曲线
(3)准确量取容量瓶中溶液10 mL加入比色皿,测得其吸光度值为0.10,则空气中二氧化硫含量为________mg·m-3.我国环境空气质量标准中对每次空气质量测定中SO2的最高浓度限值(mg/m3):一级标准:0.15二级标准:0.50三级标准:0.70.则该市空气为________级标准.
(4)甲、乙两组同学测定结果相差较大,乙组同学测定空气中SO2含量偏小,试分析乙组同学出现误差的可能原因:(两个所用药品和装置均无问题)
_______________________________________
(5)请你提出江苏防治酸雨的两条主要措施:
_______________________________________
查看答案和解析>>
科目:高中化学 来源:2013-2014学年陕西省西安市高三第四次质量检测化学试卷(解析版) 题型:实验题
氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、易水解,可用做肥料、灭火剂、洗涤剂等。某化学兴趣小组模拟制备氨基甲酸铵,并探究其分解反应平衡常数。反应的化学方程式: 2NH3(g)+CO2(g)  NH2COONH4(s)。请按要求回答下列问题:
NH2COONH4(s)。请按要求回答下列问题:
(1)请在下图1方框内画出用浓氨水与生石灰制取氨气的装置简图。
(2)制备氨基甲酸铵的装置如下图2所示。生成的氨基甲酸铵小晶体悬浮在四氯化碳中。

①从反应后的混合物中分离出产品的实验方法是_____________(填操作名称)。
②上图3中浓硫酸的作用是_______________________________________。
(3)将一定量纯净的氨基甲酸铵固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡。实验测得不同温度下的平衡数据列于下表:
|
温度(℃) |
15.0 |
20.0 |
25.0 |
30.0 |
35.0 |
|
平衡总压强(kPa) |
5.7 |
8.3 |
12.0 |
17.1 |
24.0 |
|
平衡气体总浓度(×10-3mol/L) |
2.4 |
3.4 |
4.8 |
6.8 |
9.4 |
①下列选项可以判断该分解反应达到平衡的是________。
A.
B.密闭容器内物质总质量不变
C.密闭容器中混合气体的密度不变
D.密闭容器中氨气的体积分数不变
②该分解反应的焓变ΔH______0(填 “>”、“=”或“<”),25.0℃时分解平衡常数的值=__________。
③取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25.0℃下达到分解平衡。若在恒温下压缩容器体积,氨基甲酸铵固体的质量将_________(填“增加”,“减少”或“不变”)。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年天津市河西区高三总复习质量检测(二)理综化学试卷(解析版) 题型:实验题
氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、易水解,可用做肥料、灭火剂、洗涤剂等。某化学兴趣小组模拟制备氨基甲酸铵,并探究其分解反应平衡常数。反应的化学方程式: 2NH3(g)+CO2(g)  NH2COONH4(s)。请按要求回答下列问题:
NH2COONH4(s)。请按要求回答下列问题:
(1)请在下图1方框内画出用浓氨水与生石灰制取氨气的装置简图。
(2)制备氨基甲酸铵的装置如下图2所示。生成的氨基甲酸铵小晶体悬浮在四氯化碳中。

①从反应后的混合物中分离出产品的实验方法是_____________(填操作名称)。
②上图3中浓硫酸的作用是_______________________________________。
(3)将一定量纯净的氨基甲酸铵固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积
忽略不计),在恒定温度下使其达到分解平衡。实验测得不同温度下的平衡数据列于下表:
|
温度(℃) |
15.0 |
20.0 |
25.0 |
30.0 |
35.0 |
|
平衡总压强(kPa) |
5.7 |
8.3 |
12.0 |
17.1 |
24.0 |
|
平衡气体总浓度(×10-3mol/L) |
2.4 |
3.4 |
4.8 |
6.8 |
9.4 |
①下列选项可以判断该分解反应达到平衡的是________。
A.
B.密闭容器内物质总质量不变
C.密闭容器中混合气体的密度不变
D.密闭容器中氨气的体积分数不变
②该分解反应的焓变ΔH______0(填“>”、“=”或“<”)。
25.0℃时的分解平衡常数的值=__________________________。
③取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25.0℃下达到分解平衡。若在恒温下压缩容器体积,氨基甲酸铵固体的质量将_________(填“增加”,“减少”或“不变”)。
(4)图2中反应器用冰水冷却的原因是_____________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com