
����ͼװ�ã�I��Ϊһ�ֿɳ���ص�ʾ��ͼ�����е����ӽ���Ĥֻ����K+ͨ�����õ�ص�Ļ�ѧ����ʽΪ��

��II��Ϊ���ص�ʾ��ͼ��

���պϿ���Kʱ���缫X������Һ�ȱ�졣��պ�Kʱ������˵����ȷ����
A���缫A�Ϸ����ķ�ӦΪ��2S22---2e-=S42-
B��K+���ҵ���ͨ�����ӽ���Ĥ
C���缫X�Ϸ����ķ�ӦΪ��2Cl--2e-=Cl2��
D������0��1 mol K+ͨ�����ӽ���Ĥ��Y�缫�ϲ���2��24 L���壨��״����
 Ʒѧ˫�ž�ϵ�д�
Ʒѧ˫�ž�ϵ�д� Сѧ��ĩ���100��ϵ�д�
Сѧ��ĩ���100��ϵ�д� ��ĩ��ϰ���ϵ�д�
��ĩ��ϰ���ϵ�д� ����ѧ�䵥Ԫ������ĩר����100��ϵ�д�
����ѧ�䵥Ԫ������ĩר����100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ��㶫ʡտ���б�ҵ����в������ۻ�ѧ�Ծ��������棩 ���ͣ�������
�״�����Ϊȼ�ϵ�ص�ԭ�ϡ���CH4��H2OΪԭ�ϣ�ͨ�����з�Ӧ���Ʊ��״���
I��CH4(g)+H2O(g) CO(g)+3H2(g)
��H=+206.0kJ•mol��1
CO(g)+3H2(g)
��H=+206.0kJ•mol��1
II��CO(g)+2H2(g) CH3OH(g)
��H=��129.0kJ•mol��1
CH3OH(g)
��H=��129.0kJ•mol��1
��1��CH4(g)��H2O(g)��Ӧ����CH3OH(g)��H2(g)���Ȼ�ѧ����ʽΪ ��
��2����1.0mol CH4��1.0mol H2O(g)ͨ���ݻ�Ϊ100 L�ķ�Ӧ�ң���һ�������·�����ӦI�������һ����ѹǿ��CH4��ת�������¶ȵĹ�ϵ��ͼ��
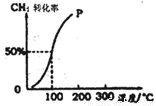
�ټ���100��ʱ�ﵽƽ�����蹹ʱ��Ϊ5min������H2��ʾ�÷�Ӧ��ƽ����Ӧ����Ϊ ��
��1000Cʱ��ӦI��ƽ�ⳣ��Ϊ ��
��3����ѹǿΪ0.1 MPa���¶�Ϊ300�������£���a molCO��2a mol H2�Ļ�������ڴ��������·�����ӦII���ɼ״���ƽ����������ݻ�ѹ����ԭ����1/2�������������䣬��ƽ����ϵ������Ӱ���� ������ĸ��ţ���
A��ƽ�ⳣ��K���� B������Ӧ���ʼӿ죬�淴Ӧ���ʼ���
C��CH3OH�����ʵ������� D������ƽ��c(H2)/c(CH3OH)��С
��4���״���ˮ�ʻ����һ������Ⱦ����һ�ֵ绯ѧ��������������Ⱦ����ԭ���ǣ�ͨ���CO2+������CO3+��Ȼ����CO3+���������ٰ�ˮ�еļ״�������CO2������������ͼװ���еĵ�ԴΪ�״���������KOH��Һ��ȼ�ϵ�أ����������ĵ缫��Ӧʽ�� ���õ�ع���ʱ����Һ�е�OH���� ���ƶ���������1mol�״���ˮ��ȼ�ϵ��ת�Ƶ��� mol��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012�������̶������һ�и�һ��ѧ������������ѧ�Ծ��������棩 ���ͣ�ʵ����
ij�о���ѧϰС����������¶���ʵ��:
��I��ʵ����֤Ԫ����������, �ǽ���Ԫ�صķǽ�����Խǿ����Ӧ����ۺ���������Ծ�Խǿ�����������ͼװ������֤����̼����Ԫ�صķǽ�����ǿ����

��Ƶ�ʵ���ֱ��֤�������������ǿ������֪A��ǿ�ᣬ�����¿���ͭ��Ӧ��B�ǿ�״���壻��Һ©���Ļ�����C�пɹ۲쵽�а�ɫ�������ɡ�
(1)д����ѡ�����ʵĻ�ѧʽ��
A�� ��B�� ��C�� ��
(2)д���ձ��з�����Ӧ�����ӷ���ʽ�� ��
(�� )Ϊ�Ƚ�Fe3+��Cu2+��H2O2�Ĵ�Ч�����ס�����λͬѧ�ֱ��������ͼһ��ͼ����ʾ��ʵ�顣
��1��ͼһ��ͨ���۲�
���ԱȽϵó����ۡ���ͬѧ�����CuSO4��ΪCuCl2��Ϊ�������������� �����߽�FeCl3 ��Һ�ij����ʵ���Ũ��Ϊ mol/L ��Fe2(SO4)3��Һ��

��2�����ͼ��װ�������Եķ����� ;
ͼ����ʾʵ����������������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ͼװ�ã�I��Ϊһ�ֿɳ���ص�ʾ��ͼ�����е����ӽ���Ĥֻ����K+ͨ�����õ�ص�Ļ�ѧ����ʽΪ��
![]()
��II��Ϊ���ص�ʾ��ͼ��
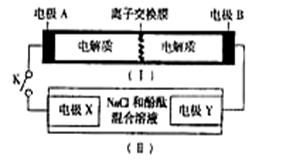
���պϿ���Kʱ���缫X������Һ�ȱ�졣��պ�Kʱ������˵����ȷ����
A���缫A�Ϸ����ķ�ӦΪ��2S22---2e-=S42-
B��K+���ҵ���ͨ�����ӽ���Ĥ
C���缫X�Ϸ����ķ�ӦΪ��2Cl--2e-=Cl2��
D������0��1 mol K+ͨ�����ӽ���Ĥ��Y�缫�ϲ���2��24 L���壨��״����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ͼװ�ã�I��Ϊһ�ֿɳ���ص�ʾ��ͼ�����е����ӽ���Ĥֻ����K+ͨ�����õ�ص�Ļ�ѧ����ʽΪ��
��II��Ϊ���ص�ʾ��ͼ��
���պϿ���Kʱ���缫X������Һ�ȱ�졣��պ�Kʱ������˵����ȷ����
A���缫A�Ϸ����ķ�ӦΪ��2S22---2e-=S42-
B��K+���ҵ���ͨ�����ӽ���Ĥ
C���缫X�Ϸ����ķ�ӦΪ��2Cl--2e-=Cl2��
D������0��1mol K+ͨ�����ӽ���Ĥ��Y�缫�ϲ���2��24 L���壨��״����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com