
【题目】用NA表示阿伏加德罗常数的值。下列判断正确的是
A. 44g N2O含有的N原子数目为NA
B. 常温常压下,22.4 L N2含有的分子数目为NA
C. 1mol Mg变为Mg2+时失去的电子数目为2NA
D. 1L 1mol·L-1 K2CO3溶液中含有的 K+ 数目为NA
科目:高中化学 来源: 题型:
【题目】利用如图所示装置(电极均为惰性电极)可吸收SO2 , 并用阴极排出的溶液吸收NO2。下列关于该装置的四种说法,正确的组合是( )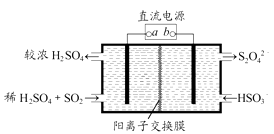
①.a为直流电源的负极
②.阴极的电极反应式为:2HSO3-+2H++2e-=S2O42-+2H2O
③.阳极的电极反应式为:SO2+2H2O-2e-=SO42-+4H+
④.电解时,H+由阴极室通过阳离子交换膜到阳极室
A.①和②
B.①和③
C.②和③
D.③和④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请回答下列问题:
(1)现有下列状态的物质①干冰 ②NaHCO3晶体 ③氨水 ④纯醋酸 ⑤FeCl3溶液⑥铜 ⑦熔融的KOH ⑧蔗糖, 其中属于电解质的是___,能导电的是___.
(2)向煮沸的蒸馏水中逐滴加入___溶液,继续煮沸至___,停止加热,可制得Fe(OH)3胶体,制取Fe(OH)3胶体化学反应方程式为___.
(3)实验室制欲用固体NaOH来配0.5mol/L的NaOH溶液500mL,配制时,一般可分为以下几个步骤:①称量②计算③溶解④摇匀⑤转移⑥洗涤⑦定容⑧冷却。其正确的操作顺序为______.在配制过程中,若其它操作均正确,下列操作会引起结果偏高的是______
A. 没有洗涤烧杯和玻璃棒 B. 未等NaOH溶液冷却至室温就转移到容量瓶中
C. 容量瓶不干燥,含有少量蒸馏水 D. 定容时俯视标线
E. 称量时间过长。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下已知:4Al(s)+3O2(g)═2Al2O3(s)△H1 , 4Fe(s)+3O2(g)═2Fe2O3(s)△H2;下面关于△H1、△H2的比较正确的是( )
A.△H1>△H2
B.△H1<△H2
C.△H1=△H2
D.无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通常工业上监测SO2含量是否达到排放标准的化学反应原理是SO2+ H2O2+ BaCl2= BaSO4↓+ 2HC1 ,用NA表示阿伏加德罗常数的值,下列说法不正确的是( )
A.0.1 molBaCl2中所含离子总数约为0.3 NA
B.25℃时,pH=l的HC1溶液中含有H+的数目约为0.1 NA
C.标准状况下,17gH2O2中所含电子总数约为9 NA
D.生成2.33gBaSO4沉淀时,吸收SO2的体积在标准状况下约为0.224L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氧化还原反应的叙述中正确的是( )
A.失去电子的反应为还原反应
B.含有氧元素的物质是氧化剂
C.氧化剂得到电子的数目和还原剂失去的电子的数目一定相等
D.氧化剂和还原剂不可能是同一种物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】观察下列实验装置图,回答问题:


(1)石灰水长时间露置于空气中,溶液表面会产生一层“膜”,“膜”物质的化学式是____,可用上图中________装置(填序号)进行相关实验操作除去膜物质。
(2)提纯含有少量NaCl的KNO3,可将混合物溶解在热水中形成饱和溶液,然后在②装置中进行蒸发浓缩,________后进行过滤、________、干燥。
(3)实验室制Cl2用装置③吸收尾气,集气瓶中可放入________溶液,尾气应从_______通入(填a、b)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于可逆反应N2(g)+3H2(g)2NH3(g)△H<0,下列研究目的和示意图相符的是( )
A | B | C | D | |
研究目的 | 压强对反应的影响(P2>P1) | 温度对反应的影响 | 平衡体系增加N2对反应的影响 | 催化剂对反应的影响 |
图示 |
|
|
|
|
A.A
B.B
C.C
D.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com