
| A. | 按照系统命名法,烃分子 的名称为2,3-二甲基-3-乙基戊烷 的名称为2,3-二甲基-3-乙基戊烷 | |
| B. | 鸡蛋白、大豆蛋白等蛋白质可溶于水,在这些蛋白质溶液中加入(NH4)2SO4或Na2SO4的浓溶液,可使蛋白质的溶解度降低而析出 | |
| C. | 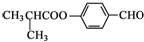 可发生加成反应、取代反应、氧化反应 可发生加成反应、取代反应、氧化反应 | |
| D. | 有机物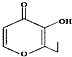 (俗称“一滴香”)的一种含苯环的同分异构体能发生银镜反应 (俗称“一滴香”)的一种含苯环的同分异构体能发生银镜反应 |
分析 A、烷烃命名时,要选最长的碳链为主链,当有多条主链可选时,要选支链多的做主链;
B、蛋白质遇浓的非重金属盐溶液会发生盐析;
C、 中含酯基、醛基和苯环;
中含酯基、醛基和苯环;
D、根据该有机物的芳香族同分异构体是否含有醛基判断.
解答 解:A、烷烃命名时,要选最长的碳链为主链,当有多条主链可选时,要选支链多的做主链,故此烷烃的主链上有5个碳原子,在2号碳原子上有一个甲基,在3号碳原子上有一个甲基和一个乙基,故名称为:2,3-二甲基-3-乙基戊烷,故A正确;
B、蛋白质遇浓的非重金属盐溶液会发生盐析,即溶解度降低而沉淀析出,故B正确;
C、 中含酯基、醛基和苯环,含醛基和苯环,故能发生加成反应;含酯基,故能发生取代反应;含醛基,故能发生氧化反应,故C正确;
中含酯基、醛基和苯环,含醛基和苯环,故能发生加成反应;含酯基,故能发生取代反应;含醛基,故能发生氧化反应,故C正确;
D、该有机物含有三个双键,其芳香族同分异构体含有苯环,所以苯环的支链上不可能含有醛基,导致其芳香族同分异构体不能发生银镜反应,故D错误.
故选D.
点评 本题考查了有机物的结构和性质,易错选项是D,能正确判断该有机物芳香族同分异构体的结构是解答本题的难点.


 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:选择题
| A. | 乙醇与浓氢溴酸反应 CH3CH2OH+HBr$\stackrel{△}{→}$CH3CH2Br+H2O | |
| B. | 溴乙烷与氢氧化钠溶液共热 CH3CH2Br+NaOH$→_{△}^{水}$CH3CH2OH+NaBr | |
| C. | 苯酚钠中通入少量的二氧化碳 2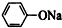 +CO2+H2O→2 +CO2+H2O→2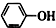 +Na2CO3 +Na2CO3 | |
| D. | 乙醛催化氧化 2CH3CHO+O2$→_{△}^{催化剂}$2CH3COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
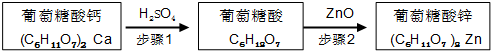
| 物质名称 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 | 氯化钙 |
| 水中的溶解性 | 可溶于冷水 易溶于热水 | 可溶 | 易溶 | 易溶 |
| 乙醇中的溶解性 | 微溶 | 微溶 | 可溶 | 可溶 |
 请回答下列问题:
请回答下列问题: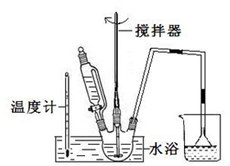
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 操作 | 现象 | 结论 | |
| A | ①滴加稀HNO3 ②滴加BaCl2溶液 | 无明显现象 白色沉淀 | 原溶液一定含Ag+ |
| B | 滴加稀盐酸 | 有大量气泡产生 | 原溶液一定含CO32- |
| C | ①滴加稀HCl ②滴加AgNO3溶液 | 无明显现象 白色沉淀 | 原溶液一定含Cl- |
| D | ①加KSCN溶液 ②滴加氯水 | 无明显现象 溶液呈红色 | 原溶液一定含Fe2+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
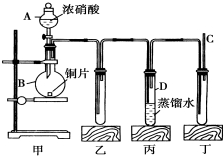 某学校化学学习小组为探究二氧化氮的性质,按如图所示装置进行实验.
某学校化学学习小组为探究二氧化氮的性质,按如图所示装置进行实验.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com