
已知当NH4Cl溶液的浓度小于0.1 mol·L-1时,其pH>5.1。现用0.1 mol·L-1的盐酸滴定10 mL 0.05 mol·L-1的氨水,用甲基橙作指示剂达到终点时所用盐酸的量应是( )
A.10 mL B.5 mL C.大于5 mL D.小于5 mL
科目:高中化学 来源: 题型:
根据下列几种物质的熔点和沸点数据,判断下列有关说法中,错误的是( )。
| NaCl | MgCl2 | AlCl3 | SiCl4 | 单质B | |
| 熔点/℃ | 810 | 710 | 190 | -68 | 2 300 |
| 沸点/℃ | 1 465 | 1 418 | 182.7 | 57 | 2 500 |
注:AlCl3熔点在2.02×105 Pa条件下测定。
A.SiCl4是分子晶体
B.单质B是原子晶体
C.AlCl3加热能升华
D.MgCl2所含离子键的强度比NaCl大
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,萘可以被硝酸和硫酸的混合酸硝化生成二硝基物,它是1,5二硝基萘 1,8二硝基萘
1,8二硝基萘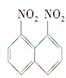 的混合物,后者可溶于质量分数大于98%的硫酸,而前者不能。利用这一性质可将这两种同分异构体分离。将上述硝化产物加入适量98%的硫酸,充分搅拌,用耐酸漏斗过滤,欲从滤液中得到固体1,8二硝基萘,应采用的方法是( )
的混合物,后者可溶于质量分数大于98%的硫酸,而前者不能。利用这一性质可将这两种同分异构体分离。将上述硝化产物加入适量98%的硫酸,充分搅拌,用耐酸漏斗过滤,欲从滤液中得到固体1,8二硝基萘,应采用的方法是( )
A.蒸发浓缩结晶 B.向滤液中加水过滤
C.用碳酸钠溶液处理滤液 D.将滤液缓缓加入水中
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是A、B两种有机物的有关信息:
| A | B |
| ①能使溴的四氯化碳溶液褪色; ②比例模型为 ③能与水在一定条件下反应 | ①由C、H两种元素组成; ②球棍模型为: |
根据表中信息回答下列问题:
(1)A与溴的四氯化碳溶液反应的生成物的名称叫做
________________________________________________________________________;
写出在一定条件下,A生成高分子化合物的化学反应方程式:
________________________________________________________________________。
(2)A与氢气发生加成反应后生成C,与C在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式CnH2n+2。当n=________时,这类有机物开始出现同分异构体。
(3)B具有的性质是________(填序号):①无色无味液体、②有毒、③不溶于水、④密度比水大、⑤能使酸性KMnO4溶液和溴水褪色、⑥任何条件下不与氢气反应。
写出在浓硫酸作用下,B与浓硝酸在60℃反应的化学方程式:
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关叙述正确的是( )
A.在中和滴定中,既可用标准溶液滴定待测溶液,也可用待测溶液滴定标准溶液
B.进行中和滴定操作时,眼睛要始终注视滴定管内溶液液面的变化
C.滴定中和热时,两烧杯间填满碎纸的作用是固定小烧杯
D.若用50 mL 0.55 mol·L-1的氢氧化钠溶液,分别与50 mL 0.50 mol·L-1的盐酸和50 mL 0.50 mol·L-1硫酸充分反应,两反应的中和热不相等
查看答案和解析>>
科目:高中化学 来源: 题型:
向1.0 L 0.30 mol·L-1的NaOH溶液中缓慢通入8.8 g CO2气体,使其完全反应,对反应后的溶液,下列判断正确的是( )
A.溶质为Na2CO3
B.溶质为NaHCO3
C.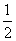 c(Na+)=c(HCO
c(Na+)=c(HCO )+c(CO
)+c(CO )+c(H2CO3)
)+c(H2CO3)
D.c(Na+)+c(H+)=c(HCO )+2c(CO
)+2c(CO )+c(OH-)
)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),使其达到分解平衡:NH2COONH4(s)  2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表:
2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表:
| 温度/℃ | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强/kPa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度/10-3mol/L | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
A 该可逆反应达到平衡的标志之一是混合气体平均相对分子质量不变
B 因该反应熵变(△S)大于0,焓变(△H)大于0,所以在低温下自发进行
C根据表中数据,计算15.0℃时的分解平衡常数约为2.0×10-9(mol·L-1)3
D达到平衡后,若在恒温下压缩容器体积,氨基甲酸铵固体的质量减小
查看答案和解析>>
科目:高中化学 来源: 题型:
有一学生在实验室测某溶液的pH。实验时,他先用蒸馏水润湿pH试纸,然后用洁净干燥的玻璃棒蘸取试样进行检测。
(1)该学生的操作是__________(填“正确”或“错误”)的,其理由是
________________________________________________________________________。
(2)如不正确,请分析是否一定有误差
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(3)若用此法分别测定[H+]相等的盐酸和醋酸溶液的pH,误差较大的是__________,原因是________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com