
| A. | Cn(H2O)m | B. | (C2O3)n(H2O)m | C. | (C2H)n(H2O)m | D. | (CO)n(H2O)m |
分析 若有机物表示为Cm(H2O)n,则消耗的氧气和生成的二氧化碳的体积比为1:1,实际为9:8,大于1:1,故有机物组成可表示为(CxHy)m(H2O)n,则(x+$\frac{y}{4}$):x=9:8,据此整理出该类化合物的通式;
解答 解若有机物表示为Cm(H2O)n,则消耗的氧气和生成的二氧化碳的体积比为1:1,实际为9:8,大于1:1,故有机物组成可表示为(CxHy)m(H2O)n,则(x+$\frac{y}{4}$):x=9:8,据此整理出该类化合物的通式,整理得x=2y,故该类化合物可以表示为(C2H)n(H2O)m,
故选C.
点评 此题的难度较大,关键是消耗氧气的体积与生成的二氧化碳的体积之比为9:8,确定有机物的分子式为(CxHy)m(H2O)n.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
| 物质 N(mol) 时间(min) | CO2 | H2 | CaO |
| 0 | 0.50 | 1.00 | 0.40 |
| 2 | 0.35 | 0.60 | a |
| 6 | 0.20 | 0.20 | b |
| 8 | 0.20 | 0.20 | b |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 治疗疟疾的青蒿素(如图),分子式为C15H20O5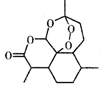 | |
| B. | 甲苯苯环上的一个氢原子被-C3H6Cl取代,形成的同分异构体有9种 | |
| C. | 对三联苯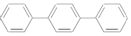 分子中至少有16个原子共平面 分子中至少有16个原子共平面 | |
| D. | 油脂和乙烯在一定条件下都能与水反应,且反应类型相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
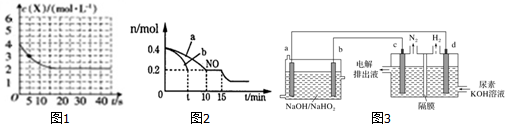
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 简单离子半径:a<c<d<e | |
| B. | 气态氢化物的稳定性e<b<c | |
| C. | 最高价氧化物的水化物酸性b>e | |
| D. | c和d形成的化合物溶于水后溶液呈碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | 组成 | 体积比 |
| 1 | ||
| 2 | ||
| 3 | ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com