
”¾ĢāÄæ”æ£Ø1£©½«ĀČ»ÆĀĮČÜŅŗÕōøÉ×ĘÉÕµĆµ½µÄ¹ĢĢåĪļÖŹŹĒ£ØĢī»ÆѧŹ½£©____________Ļņ“æ¼īČÜŅŗÖŠµĪČė¼øµĪ·ÓĢŖ»į±äŗģ£¬ŌŅņŹĒ£ØÓĆĄė×Ó·½³ĢŹ½±ķŹ¾£©_______________ ”£
£Ø2£©ŃĄ³Ż±ķĆęÓÉŅ»²ć¼įÓ²µÄ”¢×é³ÉĪŖCa5(PO4)3OHµÄĪļÖŹ±£»¤×Å”£ĖüŌŚĶŁŅŗÖŠ“ęŌŚĻĀĮŠĘ½ŗā£ŗCa5(PO4)3OH(s)![]() 5Ca2++3PO43-+OH-”£½ųŹ³ŗóĻø¾śŗĶĆø×÷ÓĆÓŚŹ³Īļ²śÉśÓŠ»śĖį£¬ÕāŹ±ŃĄ³Ż¾Ķ»įŹÜµ½øÆŹ“£¬ĘäŌŅņŹĒ_____________________________________________”£
5Ca2++3PO43-+OH-”£½ųŹ³ŗóĻø¾śŗĶĆø×÷ÓĆÓŚŹ³Īļ²śÉśÓŠ»śĖį£¬ÕāŹ±ŃĄ³Ż¾Ķ»įŹÜµ½øÆŹ“£¬ĘäŌŅņŹĒ_____________________________________________”£
£Ø3£©1gĢ¼ÓėŹŹĮæĖ®ÕōĘų·“Ӧɜ³ÉCOŗĶH2£¬ŠčĪüŹÕ10.94KJČČĮ棬“Ė·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖ_________________________________________________________
”¾“š°ø”æAl2O3 CO32-+H2O![]() HCO3-+OH- ĖįÖŠŗĶĮĖOH-£¬“Ł½ųČܽāĘ½ŗāÓŅŅĘ C£Øs)+H2O£Øg)=CO£Øg)+H2£Øg)”÷H=+131.28kJ”¤mol-1
HCO3-+OH- ĖįÖŠŗĶĮĖOH-£¬“Ł½ųČܽāĘ½ŗāÓŅŅĘ C£Øs)+H2O£Øg)=CO£Øg)+H2£Øg)”÷H=+131.28kJ”¤mol-1
”¾½āĪö”æ
£Ø1£©øł¾ŻĪĀ¶Č¶ŌĖ®½āĘ½ŗāµÄÓ°Ļģ·ÖĪö£»øł¾ŻĢ¼ĖįÄĘŹĒĒæ¼īČõĖįŃĪ£¬Ģ¼ĖįøłĖ®½ā·ÖĪö½ā“š£»
£Ø2£©ŅĄ¾ŻĶā½ēĢõ¼ž¶Ō³ĮµķČܽāĘ½ŗāµÄÓ°ĻģŅņĖŲ·ÖĪö£»
£Ø3£©øł¾Ż1gĢ¼·“Ó¦ĪüŹÕµÄČČĮæŹéŠ“·“Ó¦µÄČČ»Æѧ·½³ĢŹ½”£
£Ø1£©ĀČ»ÆĀĮĖ®½āÉś³ÉĒāŃõ»ÆĀĮŗĶŃĪĖį£¬½«ĀČ»ÆĀĮČÜŅŗ¼ÓČČÕōøÉ£¬“Ł½ųĀČ»ÆĀĮĖ®½ā£¬Ę½ŗāĻņÓŅŅĘ¶Æ£¬ŃĪĖį»Ó·¢£¬µĆµ½ĒāŃõ»ÆĀĮ¹ĢĢ壬×ĘÉÕµĆµ½Ńõ»ÆĀĮ£»Ģ¼ĖįøłĖ®½āČÜŅŗĻŌ¼īŠŌ£¬Ņņ“ĖĻņ“æ¼īČÜŅŗÖŠµĪČė¼øµĪ·ÓĢŖ»į±äŗģ£¬Ė®½āµÄĄė×Ó·½³ĢŹ½ĪŖCO32-+H2O![]() HCO3-+OH-£»
HCO3-+OH-£»
£Ø2£©Ca5(PO4)3OHŌŚĶŁŅŗÖŠ“ęŌŚĻĀĮŠĘ½ŗā·“Ó¦£ŗCa5(PO4)3OH(s)![]() 5Ca2++3PO43-+OH-£¬½ųŹ³ŗóĻø¾śŗĶĆø×÷ÓĆÓŚŹ³Īļ²śÉśÓŠ»śĖį£¬ÓŠ»śĖįÓėOH-·“Ó¦£¬H++OH-=H2O£¬Ź¹³ĮµķČܽāĘ½ŗāĻņÓŅŅĘ¶Æ£¬µ¼ÖĀCa5(PO4)3OHČܽā£¬Ōģ³ÉČ£³Ż£»
5Ca2++3PO43-+OH-£¬½ųŹ³ŗóĻø¾śŗĶĆø×÷ÓĆÓŚŹ³Īļ²śÉśÓŠ»śĖį£¬ÓŠ»śĖįÓėOH-·“Ó¦£¬H++OH-=H2O£¬Ź¹³ĮµķČܽāĘ½ŗāĻņÓŅŅĘ¶Æ£¬µ¼ÖĀCa5(PO4)3OHČܽā£¬Ōģ³ÉČ£³Ż£»
£Ø3£©1gĢ¼ÓėŹŹĮæĖ®ÕōĘų·“Ӧɜ³ÉCOŗĶH2£¬ŠčĪüŹÕ10.94kJČČĮ棬Ņņ“Ė1molĢ¼¼“12gĢ¼ĶźČ«Č¼ÉÕĪüŹÕµÄČČĮæŹĒ12”Į10.94kJ£½131.28kJ”¤mol-1£¬Ōņ“Ė·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖC£Øs)+H2O£Øg)£½CO£Øg)+H2£Øg)”÷H=+131.28 kJ”¤mol-1”£


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijŹµŃéŹŅ²śÉśµÄ·ĻŅŗÖŠŗ¬ÓŠFe3+”¢Cu2+”¢Ba2+ČżÖÖ½šŹōĄė×Ó£¬ŃŠ¾æŠ”×éÉč¼ĘĮĖĻĀĮŠ·½°ø¶Ō·ĻŅŗ½ųŠŠ“¦Ąķ£¬ŅŌ»ŲŹÕ½šŹō£¬±£»¤»·¾³”£

Ēė»Ų“š£ŗ
(1)²½Öč¢Ł¢Ś¢ÜÓƵ½µÄÖ÷ŅŖ²£Į§ŅĒĘ÷ŹĒ___________________”£
(2)²½Öč¢ŪµÄŹµŃéĻÖĻóŹĒ_________________”£
(3) Éč¼ĘŅ»øöŹµŃé·½°ø£¬ŃéÖ¤²½Öč¢ŁÖŠĖł¼ÓĮņĖįČÜŅŗ¼ŗ¾¹żĮæ____________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ³£ĪĀĻĀ£¬ÓĆ0.10 mol”¤L£1 NaOHČÜŅŗ·Ö±šµĪ¶Ø20.00 mLÅØ¶Č¾łĪŖ0.10 mol”¤L£1 CH3COOHČÜŅŗŗĶHCNČÜŅŗ£¬ĖłµĆµĪ¶ØĒśĻßČēĻĀĶ¼”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ

A. µć¢ŁŗĶµć¢ŚĖłŹ¾ČÜŅŗÖŠ£ŗc(CH3COO£)£¼c(CN£)
B. µć¢ŪŗĶµć¢ÜĖłŹ¾ČÜŅŗÖŠ£ŗc(Na£«)£¾c(OH£)£¾c(CH3COO£)£¾c(H£«)
C. µć¢ŁŗĶµć¢ŚĖłŹ¾ČÜŅŗÖŠ£ŗc(CH3COO£)£c(CN£)£½c(HCN)£c(CH3COOH)
D. µć¢ŚŗĶµć¢ŪĖłŹ¾ČÜŅŗÖŠ¶¼ÓŠ£ŗc(CH3COO£)£«c(OH£)£½c(CH3COOH)£«c(H£«)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”ææÉŅŌ³ä·ÖĖµĆ÷·“Ó¦P£Øg£©+Q£Øg£©![]() R£Øg£©+S£Øg£©ŌŚŗćĪĀĻĀŅŃ“ļµ½Ę½ŗāµÄŹĒ
R£Øg£©+S£Øg£©ŌŚŗćĪĀĻĀŅŃ“ļµ½Ę½ŗāµÄŹĒ
A. ·“ӦȯĘ÷ÄŚµÄŃ¹Ēæ²»Ėꏱ¼äøıä
B. ·“ӦȯĘ÷ÄŚP”¢Q”¢R”¢SĖÄÕßÅضČÖ®±ČĪŖ1:1:1:1
C. PµÄÉś³ÉĖŁĀŹŗĶSµÄÉś³ÉĖŁĀŹĻąµČ
D. ·“ӦȯĘ÷ÄŚµÄĘųĢå×ÜĪļÖŹµÄĮæ²»Ėꏱ¼ä±ä»Æ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ5©¶ž¼×Ńõ»ł±½·ÓŹĒÖŲŅŖµÄÓŠ»śŗĻ³ÉÖŠ¼äĢ壬æÉÓĆÓŚĢģČ»ĪļÖŹ°×ÄūĆŹĖŲµÄŗĻ³É£¬Ņ»ÖÖŅŌ¼ä±½Čż·ÓĪŖŌĮĻµÄŗĻ³É·“Ó¦ČēĻĀ£ŗ

¼×“¼”¢ŅŅĆŃŗĶ3£¬5©¶ž¼×Ńõ»ł±½·ÓµÄ²æ·ÖĪļĄķŠŌÖŹ¼ūĻĀ±ķ£ŗ
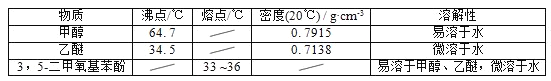
£Ø1£©·“Ó¦½įŹųŗó£¬ĻČ·ÖĄė³ö¼×“¼£¬ŌŁ¼ÓČėŅŅĆŃ½ųŠŠŻĶČ”£¬¢Ł·ÖĄė³ö¼×“¼µÄ²Ł×÷ŹĒµÄ______£»¢ŚŻĶČ”ÓƵ½µÄ·ÖŅŗĀ©¶·Ź¹ÓĆĒ°Šč__________________²¢Ļ“¾»£¬·ÖŅŗŹ±ÓŠ»ś²ćŌŚ·ÖŅŗĀ©¶·µÄ________Ģī£Ø”°ÉĻ”±»ņ”°ĻĀ”±£©²ć£»
£Ø2£©·ÖĄėµĆµ½µÄÓŠ»ś²ćŅĄ“ĪÓƱ„ŗĶNaHCO3ČÜŅŗ”¢±„ŗĶŹ³ŃĪĖ®”¢ÉŁĮæÕōĮóĖ®½ųŠŠĻ“µÓ£®ÓƱ„ŗĶNaHCO3ČÜŅŗĻ“µÓµÄÄæµÄŹĒ__£¬ÓƱ„ŗĶŹ³ŃĪĖ®Ļ“µÓµÄÄæµÄŹĒ______£»
£Ø3£©Ļ“µÓĶź³Éŗó£¬ĶعżŅŌĻĀ²Ł×÷·ÖĄė”¢Ģį“æ²śĪļ£¬ÕżČ·µÄ²Ł×÷Ė³ŠņŹĒ__£ØĢī×ÖÄø£©£»
a£®ÕōĮó³żČ„ŅŅĆŃ b£®ÖŲ½į¾§ c£®¹żĀĖ³żČ„øÉŌļ¼Į d£®¼ÓČėĪŽĖ®CaCl2øÉŌļ
£Ø4£©¹ĢŅŗ·ÖĄė³£²ÉÓĆ¼õŃ¹¹żĀĖ£®ĪŖĮĖ·ĄÖ¹µ¹Īü£¬¼õŃ¹¹żĀĖĶź³ÉŗóÓ¦ĻČ________________£¬ŌŁ______”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”ææĘѧ¼ŅŗĻ³É³öĮĖŅ»ÖÖŠĀ»ÆŗĻĪļ(ČēĶ¼ĖłŹ¾)£¬ĘäÖŠW”¢X”¢Y”¢ZĪŖĶ¬Ņ»¶ĢÖÜĘŚŌŖĖŲ£¬ZŗĖĶā×īĶā²ćµē×ÓŹżŹĒXŗĖĶāµē×ÓŹżµÄŅ»°ė”£ĻĀĮŠŠšŹö²»ÕżČ·µÄŹĒ
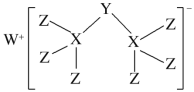
A.WµÄ×īøß¼ŪŃõ»ÆĪļŹĒĄė×Ó»ÆŗĻĪļ
B.øĆŠĀ»ÆŗĻĪļÖŠXĀś×ć8µē×ÓĪČ¶Ø½į¹¹
C.ŌŖĖŲ·Ē½šŹōŠŌµÄĖ³ŠņĪŖX£¾Y£¾Z
D.ZµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļŹĒĒæĖį
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÄÜŌ“ÓėČĖĄąµÄÉś“ęŗĶ·¢Õ¹Ļ¢Ļ¢Ļą¹Ų£¬»Æѧ·“Ó¦ŌŚČĖĄąĄūÓĆÄÜŌ“µÄĄśŹ·¹ż³ĢÖŠ³äµ±ÖŲŅŖµÄ½ĒÉ«”£»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©æĘѧ¼Ņ×ī½üŃŠÖĘ³öĄūÓĆĢ«ŃōÄܲśÉś¼¤¹ā£¬Ź¹ŗ£Ė®·Ö½ā”£Ģ«Ńō¹ā·Ö½āŗ£Ė®Ź±£¬¹āÄÜ×Ŗ»ÆĪŖ________ÄÜ£¬Ė®·Ö½āŹ±¶ĻĮѵĻÆѧ¼üŹĒ________£ØĢī”°Ąė×Ó¼ü”±»ņ”°¹²¼Ū¼ü”±£©
£Ø2£©ĒāÄÜŹĒŅ»ÖÖ¾ßÓŠ·¢Õ¹Ē°¾°µÄĄķĻėĒå½ąÄÜŌ“,ĒāĘųČ¼ÉÕŹ±·Å³ö“óĮæµÄČČ”£Čō¶ĻæŖ1molĒāĘųÖŠµÄ»Æѧ¼üĻūŗĵÄÄÜĮæĪŖQ1kJ£¬¶ĻæŖ1molŃõĘųÖŠµÄ»Æѧ¼üĻūŗĵÄÄÜĮæĪŖQ2kJ£¬ŠĪ³É1molĖ®ÖŠµÄ»Æѧ¼üŹĶ·ÅµÄÄÜĮæĪŖQ3kJ£¬ŌņĻĀĮŠ¹ŲĻµÕżČ·µÄŹĒ____________
A£®Q1£«Q2£¼Q3 B£®2Q1£«Q2£¼2Q3
C£®2Q1£«Q2£¾2Q3 D£®Q1£«Q2£¾Q3
£Ø3£©ĻĀĮŠ»Æѧ·“Ó¦ŌŚĄķĀŪÉĻæÉŅŌÉč¼Ę³ÉŌµē³ŲµÄŹĒ________”£
A.Fe+2FeCl3£½3FeCl2 B.SO3+H2O£½H2SO4
C.C+H2O![]() CO+H2 D.Ba(OH)2+H2SO4£½BaSO4+2H2O
CO+H2 D.Ba(OH)2+H2SO4£½BaSO4+2H2O
£Ø4£©ĆĄ¹śNASAŌųæŖ·¢Ņ»ÖÖĢś”¤æÕĘųµē³Ų£¬ĘäŌĄķČēĶ¼ĖłŹ¾£¬µē³Ų·“Ó¦ĪŖ£ŗ2Fe+O2+2H2O=2Fe(OH)2”£

¢Łµē¼«aĪŖŌµē³ŲµÄ________£ØĢī”°Õż¼«”±»ņ”°øŗ¼«”±£©£¬øĆ¼«µÄµē¼«·“Ó¦Ź½ĪŖ______________________£»µē¼«bÉĻ·¢Éś________·“Ó¦£ØĢī”°Ńõ»Æ”±»ņ”°»¹Ō”±£©”£
¢ŚŌµē³Ų¹¤×÷Ņ»¶ĪŹ±¼äŗó£¬ČōĻūŗÄĢś22.4g£¬ŌņµēĀ·ÖŠĶعżµÄµē×ÓŹżĪŖ________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ(1)»³öĻĀĮŠŌŖĖŲµÄŌ×Ó½į¹¹Ź¾ŅāĶ¼”£
¢ŁŗĖµēŗÉŹżĪŖ13µÄŌŖĖŲ£ŗ_______”£
¢Ś×īĶā²ćµē×ÓŹżµČÓŚ“ĪĶā²ćµē×ÓŹżµÄŌŖĖŲŌ×Ó£ŗ______”£
(2)ĻÖÓŠĮ£×Ó£ŗ1H”¢35Cl”¢2H”¢14N”¢2H37Cl£¬ĘäÖŠ£ŗ
¢ŁÓŠ_________ÖÖŌŖĖŲ£»
¢Ś__________Ö®¼ä»„³ĘĶ¬Ī»ĖŲ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ»Æѧ·“Ó¦ÖŠ£¬ŹōÓŚŃõ»Æ»¹Ō·“Ó¦µÄŹĒ
A.Al2O3+6HCl=2AlCl3+3H2O
B.Cu+2H2SO4(ÅØ)![]() CuSO4+2H2O+SO2”ü
CuSO4+2H2O+SO2ӟ
C.2NaHCO3![]() Na2CO3+CO2ӟ+H2O
Na2CO3+CO2ӟ+H2O
D.SiO2+2NaOH£½Na2SiO3+H2O
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com