
| A£® | µē½ā±„ŗĶŹ³ŃĪĖ®£ŗ2Cl-+2H2O$\frac{\underline{\;Ķصē\;}}{\;}$2OH-+H2”ü+Cl2”ü | |
| B£® | ĮņĖįļ§Ļ”ČÜŅŗŗĶĻ”ĒāŃõ»Æ±µČÜŅŗ·“Ó¦£ŗNH4++SO42-+Ba2++OH-ØTBaSO4”ż+NH3•H2O | |
| C£® | °ŃĀČĘųĶØČėNaOH ČÜŅŗÖŠ£ŗCl2+2OH-ØTCl-+ClO-+2H2O | |
| D£® | Ģ¼ĖįĒāøĘČÜŅŗÖŠ¼ÓČėÉŁĮæµÄĒāŃõ»ÆÄĘ£ŗCa2++HCO3-+OH-ØTH2O+CaCO3”ż |
·ÖĪö A£®µē½ā±„ŗĶŹ³ŃĪĖ®Éś³ÉĒāŃõ»ÆÄĘ”¢ĀČĘųŗĶĒāĘų£»
B£®ļ§øłĄė×Ó”¢ĒāŃõøłĄė×ӵļĘĮæŹż“ķĪó£»
C£®ĀČĘųÓėĒāŃõ»ÆÄĘČÜŅŗ·“Ӧɜ³ÉĀČ»ÆÄĘ”¢“ĪĀČĖįÄĘŗĶĖ®£»
D£®ĒāŃõ»ÆÄĘÉŁĮ棬·“Ӧɜ³ÉĢ¼ĖįøĘ³ĮµķŗĶĢ¼ĖįĒāÄĘ£®
½ā“š ½ā£ŗA£®µē½ā±„ŗĶŹ³ŃĪĖ®Éś³ÉNaOH”¢ĒāĘųŗĶĀČĘų£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ2Cl-+2H2O$\frac{\underline{\;Ķصē\;}}{\;}$2OH-+H2”ü+Cl2”ü£¬¹ŹAÕżČ·£»
B£®ĮņĖįļ§Ļ”ČÜŅŗŗĶĻ”ĒāŃõ»Æ±µČÜŅŗ·“Ӧɜ³ÉĮņĖį±µ³ĮµķŗĶŅ»Ė®ŗĻ°±£¬ÕżČ·µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ2NH4++SO42-+Ba2++2OH-ØTBaSO4”ż+2NH3•H2O£¬¹ŹB“ķĪó£»
C£®°ŃĀČĘųĶØČėNaOH ČÜŅŗÖŠ£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗCl2+2OH-ØTCl-+ClO-+2H2O£¬¹ŹCÕżČ·£»
D£®Ģ¼ĖįĒāøĘČÜŅŗÖŠ¼ÓČėÉŁĮæµÄĒāŃõ»ÆÄĘ£¬Ģ¼ĖįĒāøłĄė×Ó²æ·Ö·“Ó¦£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗCa2++HCO3-+OH-ØTH2O+CaCO3”ż£¬¹ŹDÕżČ·£»
¹ŹŃ”B£®
µćĘĄ Ģāæ¼²éĮĖĄė×Ó·½³ĢŹ½µÄÅŠ¶Ļ£¬ĢāÄæÄŃ¶Č²»“ó£¬×¢ŅāÕĘĪÕĄė×Ó·½³ĢŹ½µÄŹéŠ“ŌŌņ£¬Ć÷Č·Ąė×Ó·½³ĢŹ½ÕżĪóÅŠ¶Ļ³£ÓĆ·½·Ø£ŗ¼ģ²é·“Ó¦Īļ”¢Éś³ÉĪļŹĒ·ńÕżČ·£¬¼ģ²éø÷ĪļÖŹ²š·ÖŹĒ·ńÕżČ·£¬ČēÄŃČÜĪļ”¢Čõµē½āÖŹµČŠčŅŖ±£Įō»ÆѧŹ½£¬¼ģ²éŹĒ·ń·ūŗĻŌ»Æѧ·½³ĢŹ½µČ£»ŹŌĢāÓŠĄūÓŚĢįøßѧɜµÄĮé»īÓ¦ÓĆÄÜĮ¦£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ʤ·ōÉĻ²»É÷Õ“ÉĻÅØNa OHČÜŅŗ£¬Į¢¼“ÓĆĻ”ĮņĖį³åĻ“ | |
| B£® | “óĮæĀČĘųŠ¹Ā©Ź±£¬Ó¦ŃøĖŁĄėæŖĻÖ³”£¬²¢¾”æģĶłøß“¦Č„ | |
| C£® | ²»É÷Č÷³öµÄ¾Ę¾«ŌŚ×ĄÉĻ×Å»šŹ±£¬Į¢¼“ÓĆ“óĮæĖ®ĘĖĆš | |
| D£® | ½šŹōÄĘ×Å»šŹ±£¬Ó¦Į¢¼“ÓĆÕ“Ė®µÄĆ«½ķø²øĒ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
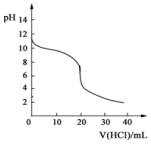 ³£ĪĀĻĀ£¬Ļņ20.00mL0.1000mol•L-1µÄ°±Ė®ÖŠÖšµĪ¼ÓČė0.1000mol•L-1µÄŃĪĖį£¬pHĖęŃĪĖįĢå»żµÄ±ä»ÆČēĶ¼ĖłŹ¾£®£Ø²»æ¼ĀĒNH3µÄŅŻ³ö£©£®ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©
³£ĪĀĻĀ£¬Ļņ20.00mL0.1000mol•L-1µÄ°±Ė®ÖŠÖšµĪ¼ÓČė0.1000mol•L-1µÄŃĪĖį£¬pHĖęŃĪĖįĢå»żµÄ±ä»ÆČēĶ¼ĖłŹ¾£®£Ø²»æ¼ĀĒNH3µÄŅŻ³ö£©£®ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©| A£® | ·“Ó¦¹ż³ĢÖŠ£ŗc£ØNH4+£©+c£ØH+£©=c£ØOH-£©+c£ØCl-£© | |
| B£® | V£ØHCl£©=10.00mLŹ±£¬c£ØNH4+£©£¾c£ØCl-£©£¾c£ØNH3•H2O£© | |
| C£® | V£ØHCl£©£¼20.00mLŹ±£¬ČÜŅŗŅ»¶Ø³Ź¼īŠŌ | |
| D£® | V£ØHCl£©=30.00mLŹ±£¬2c£ØCl-£©=3c£ØNH4+£©+3c£ØNH3•H2O£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ±ąŗÅ | ŹŌ¼Į | ±£“ę·½·Ø | ĄķÓÉ |
| A | Ė®²£Į§ | “ę·ÅŌŚ“ųĻšĘ¤ČūµÄĻøæŚĘæÖŠ£¬ĆÜ·ā | ·ĄÖ¹ÓėæÕĘų½Ó“„±»Ńõ»ÆŗĶÓė¶žŃõ»ÆĢ¼½Ó“„¶ų±äÖŹ |
| B | ĮņĖįŃĒĢś¾§Ģå | “ę·ÅŌŚ“ų²£Į§ČūµÄ¹ćæŚĘæÖŠ£¬ĆÜ·ā | ·ĄÖ¹ÓėæÕĘų½Ó“„±»Ńõ»Æ |
| C | ÅØĮņĖį | Ćܱձ£“ę | ·ĄÖ¹ĪüĖ®ŗĶ»Ó·¢ |
| D | ŠĀÖʵÄäåĖ® | “ę·ÅŌŚĪŽÉ«ŹŌ¼ĮĘæÖŠ£¬ĆÜ·ā | ·ĄÖ¹»Ó·¢ |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | SiO2+CaO=CaSiO3 | |
| B£® | SiO2+2NaOH=Na2SiO3+H2O | |
| C£® | SiO2+2C$\frac{\underline{\;øßĪĀ\;}}{\;}$Si+2CO | |
| D£® | SiO2+2Na2CO3$\frac{\underline{\;øßĪĀ\;}}{\;}$Na2SiO3+CO2”ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĮņĖįµÄµēĄė·½³ĢŹ½£ŗH2SO4=H2++SO42- | |
| B£® | ¹āµ¼ĻĖĪ¬Ö÷ŅŖ³É·ÖµÄ»ÆѧŹ½£ŗSi | |
| C£® | ÖŹ×ÓŹżĪŖ53£¬ÖŠ×ÓŹżĪŖ78µÄµāŌ×Ó£ŗ${\;}_{53}^{131}$I | |
| D£® | ÄĘĄė×ӵĽį¹¹Ź¾ŅāĶ¼£ŗ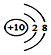 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
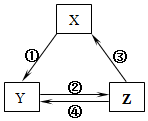 ±ķĖłĮŠø÷×éĪļÖŹÖŠ£¬ĪļÖŹÖ®¼äĶعżŅ»²½·“Ó¦¾ĶÄÜŹµĻÖČēĶ¼ĖłŹ¾×Ŗ»ÆĒŅĖłøų·“Ó¦Ģõ¼žÕżČ·µÄŹĒ£Ø””””£©
±ķĖłĮŠø÷×éĪļÖŹÖŠ£¬ĪļÖŹÖ®¼äĶعżŅ»²½·“Ó¦¾ĶÄÜŹµĻÖČēĶ¼ĖłŹ¾×Ŗ»ÆĒŅĖłøų·“Ó¦Ģõ¼žÕżČ·µÄŹĒ£Ø””””£©| Ń”Ļī | X | Y | Z | ¼żĶ·ÉĻĖł±źŹż×ֵķ“Ó¦Ģõ¼ž |
| A | SiO2 | Na2SiO3 | H2SiO3 | ¢ŁÓėNa2CO3ČŪČŚ |
| B | Na | Na2O2 | NaCl | ¢Ś¼ÓH2O |
| C | NO | NO2 | HNO3 | ¢ŪÓėC¼ÓČČ |
| D | Al2O3 | NaAlO2 | Al£ØOH£©3 | ¢ÜÓėNaOH |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÉżĪĀ | B£® | ¼õŠ”ĘųĢåŃ¹Ēæ | ||
| C£® | Ōö“ó·“Ó¦ĪļµÄÅØ¶Č | D£® | Ź¹ÓĆ“ß»Æ¼Į |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £®
£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com