
“嫦娥一号”探测器所用的镍氢蓄电池,其负极板材料M为能吸收氢原子的合金。充电时电极反应分别为:M + H2O + e-= MH + OH-,Ni(OH)2 + OH-- e-= NiOOH + H2O。
下列有关镍氢蓄电池的说法正确的是
A.放电时,正极附近的pH减小
B.放电时,总反应为MH + NiOOH = M + Ni(OH)2
C.充电时,电极M应与充电电源正极相连
D.充电后,负极板材料M变成了MH,MH中H元素显-1价
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源:2016届福建省莆田市高三上学期期中测试化学试卷(解析版) 题型:选择题
实验发现,298 K时,在FeCl3酸性溶液中加少量锌粒后,Fe3+立即被还原成Fe2+。某夏令营兴趣小组根据该实验事实设计了如图所示原电池装置。下列有关说法正确的是

A.该原电池的正极反应是Zn-2e-=Zn2+
B.左烧杯中溶液的血红色逐渐褪去
C.该电池铂电极上有气泡出现
D.该电池总反应为3Zn+2Fe3+=2Fe+3Zn2+
查看答案和解析>>
科目:高中化学 来源:2016届河南省南阳市高三上学期第一次联考化学试卷(解析版) 题型:选择题
类推的思维方法在化学学习与研究中常会产生错误的结论,因此类推的结论最终要经过实践的检验才能确定其是否正确。下列几种类推结论中正确的是
A.由2Cu+O2 2CuO可推出同族的硫也有Cu+S
2CuO可推出同族的硫也有Cu+S CuS
CuS
B.Fe3O4可表示为FeO·Fe2O3,则Pb3O4可表示为PbO·Pb2O3
C.Na能与水反应生成H2,K、Ca也能与水反应生成H2
D.CO2与Na2O2反应只生成Na2CO3和O2,故SO2与Na2O2反应只生成Na2SO3和O2
查看答案和解析>>
科目:高中化学 来源:2016届山东省淄博市高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列表示对应化学反应的离子方程式正确的是
A.用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O=3I2+6OH-
B.向NH4HSO3溶液中加过量的NaOH溶液并加热:NH4++OH- NH3↑+H2O
NH3↑+H2O
C.将过量SO2通入冷氨水中:SO2+NH3·H2O=HSO3-+NH4+
D.Ba(OH)2溶液中逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的OH-恰好反应一半时:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O
查看答案和解析>>
科目:高中化学 来源:2016届四川省广元市高三上学期第二次阶段测理综化学试卷(解析版) 题型:填空题
对金属制品进行抗腐蚀处理,可延长其使用寿命。
(1)利用如图装置,可以模拟铁的电化学防护。

若X为碳棒,为减缓铁的腐蚀,开关K应置于________处。若X为锌,开关K置于M处,该电化学防护法称为__________________。
(2)以下为铝材表面处理的一种方法:

①碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出,原因是_________________(用离子方程式表示)。为将碱洗槽液中的铝以沉淀形式回收,最好向槽液中加入下列试剂中的________。
a.NH3 b.CO2 c.NaOH d.HNO3
②以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极电极反应式为_________________。
取少量废电解液,加入NaHCO3溶液后产生气泡和白色沉淀,产生沉淀的原因是____________________。
(3)镀铜可防止铁制品腐蚀,电镀时阳极材料为________________,用铜而不用石墨作阳极的原因是______________________。
查看答案和解析>>
科目:高中化学 来源:2016届四川省广元市高三上学期第二次阶段测理综化学试卷(解析版) 题型:选择题
化学在生产和日常生活中有着重要的应用。下列说法正确的是
A.人类利用的能源都是通过化学反应获得的
B.电解熔融氯化钠,可制得金属钠
C.金属表面形成的氧化物都能起到保护内层金属的作用
D.在铁水闸上外接电源的正极,可保护铁水闸
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省龙海市高一上学期期中测试化学试卷(解析版) 题型:选择题
某元素一价阴离子的核外有18个电子,质量数为35,该微粒符号可表示为
A.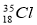 - B.
- B. C.
C. - D.
- D. -
-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高二上学期期中测试化学试卷(解析版) 题型:填空题
某温度时在2L容器中X、Y、Z三种气态物质的物质的量(n)随时间(t)变化的曲线如图所示,由图中数据分析:

(1)该反应的化学方程式为:
(2)反应开始至2min,用X表示的平均反应速率为:
(3)下列叙述能说明上述反应达到化学平衡状态的是 (填字母)
A.混合气体的总物质的量不随时间的变化而变化
B.单位时间内每消耗3mol X,同时生成2mol Z
C.混合气体的总质量不随时间的变化而变化
(4)在密闭容器里,通入a mol H2(g)和bmol I2,发生反应H2 (g)+ I2 (g)=2HI(g),当改变下列条件时,反应速率会发生什么变化(选填“增大”、“减小”或“不变”)
① 降低温度: ②保持容器的体积不变,增加X(g)的物质的量:
③ 增大容器的体积: ④容器容积不变,通入氖气________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省许昌、襄城、长葛三校高一上期中测试化学试卷(解析版) 题型:填空题
有一固体混合物,可能由Na2CO3、Na2SO4、Fe2(SO4)3、NaCl等混合而成,为检验它们,做了以下实验:
①将固体混合物溶于水中,搅拌后得无色透明溶液;
②往此溶液中滴加过量的硝酸钡溶液,有白色沉淀产生;
③过滤,将沉淀物置于足量稀硝酸中,发现沉淀部分溶解。
根据上述实验事实,回答下列问题:
(1)原固体混合物中一定含有的物质是______________,一定不含有的物质是______________,可能含有的物质是______________。对可能含有的物质,可采用向滤液中滴加______________溶液的方法来检验。(以上空格均填写化学式)
(2)写出步骤③中的离子方程式:__________________________
(3)硫酸铁在水溶液中的电离方程式________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com