
设NA为阿伏加德罗常数的值.下列说法正确的是( )
|
| A. | 标准状况下,40g SO3的体积为11.2L |
|
| B. | 高温下,0.2molFe与足量水蒸气反应,生成的H2分子数目为0.3 NA |
|
| C. | 5NH4NO3 |
|
| D. | 56g铁片投入足量浓H2SO4中生成NA个SO2分子 |
| 阿伏加德罗常数.. | |
| 分析: | A、标准状况下,SO3不是气体; B、根据化学反应方程式进行分析计算; C、5NH4NO3 D、铁与浓硫酸发生钝化,阻止了反应的继续进行,无法计算生成的二氧化硫的物质的量. |
| 解答: | 解:A、标准状况下,40gSO3的体积不能根据V=nVm=22.4n来计算,故A错误; B、红热的铁与水蒸气可发生反应:3Fe+4H2O(g) C、5NH4NO3 D、56g铁的物质的量为1mol,由于铁与浓硫酸能够发生钝化,阻止了反应的进行,无法计算反应生成二氧化硫的物质的量,故D错误; 故选C. |
| 点评: | 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标况下气体摩尔体积的使用条件,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系;试题有利于提高学生灵活运用基础知识解决实际问题的能力. |


科目:高中化学 来源: 题型:
现欲用碳酸钙固体和稀盐酸反应制取CO2气体。请回答下列问题。
(1)写出发生反应的离子方程式:_________________________________________。
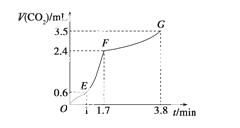
(2)实验过程中绘制出生成CO2的体积V(CO2)与时间t的关系如下图所示。试分析判断OE段、EF段、FG段反应速率[分别用v(OE)、v(EF)、v(FG)表示]的大小关系为____________;比较OE段和EF段,说明EF段速率变化的主要原因:
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关元素的性质及其递变规律正确的是( )
|
| A. | ⅠA族与ⅦA族元素间可形成共价化合物或离子化合物 |
|
| B. | 第二周期元素从左到右,最高正价从+1递增到+7 |
|
| C. | 同主族元素的简单阴离子还原性越强,水解程度越大 |
|
| D. | 同周期金属元素的化合价越高,其原子失电子能力越强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
用下图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应。下列实验不合理的是 ( )
A.上下移动①中铜丝可控制SO2的量
B.②中选用品红溶液验证SO2的生成
C.③中选用NaOH溶液吸收多余的SO2
D.为确认CuSO4生成,向①加水,观察颜色
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D四种元素都是短周期元素,A元素的离子具有黄色的焰色反应。B元素的离子结构和Ne具有相同的电子层排布;5.8 g B的氢氧化物恰好能与100 mL 2 mol・L―1盐酸完全反应;B原子核中质子数和中子数相等。H2在C单质中燃烧产生苍白色火焰。D元素原子的电子层结构中,最外层电子数是次外层电子数的3倍。根据上述条件回答:
(1)元素C位于第__________周期第__________族,它的最高价氧化物的化学式为____________。
(2)A元素是_________,B元素是________,D元素是_______。(填名称)
(3)A与D形成稳定化合物的电子式是_____________,判断该化合物在空气中是否变质的简单方法是_______________________________。
(4)C元素的单质有毒,可用A的最高价氧化物对应的水化物的溶液吸收,其离子方程式为___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
①漂白粉、水玻璃和铝热剂都是混合物;
②煤的干馏和石油的分馏都是化学变化;
③氨基酸、纯碱、芒硝和生石灰分别属于酸、碱、盐和氧化物;
④非极性键也可能存在于离子化合物中.
|
| A. | ①④ | B. | ①③ | C. | ②④ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
a molNa2O2和b molNaHCO3固体混合后,在密闭容器中加热到250℃,使其充分反应,当排出气体为两种气体时,a:b不可能为( )
|
| A. | 3:4 | B. | 4:5 | C. | 2:3 | D. | 3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中不正确的是
A.HF稳定性比HCl强 B.Mg失电子能力比Ca弱
C.NaCl与NH4Cl含有的化学键类型相同 D.等物质的量的C2H6和H2O2含电子数相同
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关说法中,正确的是 ( )
A.糖类、蛋白质在一定条件下都能发生水解反应。
B.洗衣粉、橡胶、阿司匹林都只能由人工合成得到。
C.稀双氧水可用于清洗伤口,以达到杀菌、消毒的目的。
D.变质的油脂有难闻的特殊气味,是因为油脂发生了水解反应。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com