
【题目】不可能通过观察法了解的金属钠的性质是 ( )
A.钠是一种银白色金属
B.熔点为97.81 ℃,密度为0.97 g·cm-3
C.钠与H2O剧烈反应
D.钠室温下氧化和在空气中燃烧得到不同的产物
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】高分子化合物材料PET聚酯和PMMA的合成路线如图: 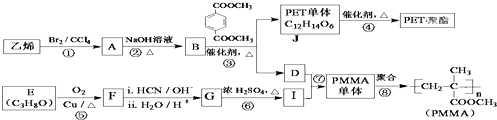
已知:
Ⅰ.RCOOR′+R″ ![]() OH
OH ![]() RCO18OR″+R′OH(R、R′、R″代表烃基)
RCO18OR″+R′OH(R、R′、R″代表烃基)
Ⅱ. ![]()
![]()
 (R、R′代表烃基)
(R、R′代表烃基)
(1)PMMA单体的化学名称 .
(2)F的核磁共振氢谱显示只有一组峰,⑤的化学方程式为 .
反应⑤、⑥的反应类型、
(3)G的分子式 , G中官能团的名称、
2分子G可形成环状化合物,写出化学方程式 .
(4)I的某种同分异构体与I具有相同官能团,且为顺式结构,其结构简式是 .
(5)写出与F互为同分异构体且含单官能团的所有有机物的结构简式 .
(6)写出由PET单体制备PET聚酯并生成B的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向盛有50mL pH=2的HA溶液的绝热容器中加入pH=13的NaOH溶液,加入NaOH溶液的体积(V)与所得混合溶液的温度(T)的关系如图所示.下列叙述正确的是( ) 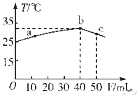
A.HA溶液的物质的量浓度为0 0l mol.L﹣1
B.b→c的过程中,温度降低的原因是溶液中发生了吸热反应
C.a→b的过程中,混合溶液中可能存在:c(A﹣)=c(Na+)
D.25℃时,HA的电离平衡常数K约为1.43×10﹣2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+B(g)C(g)+D(g)发生过程中的能量变化如图,△H 表示反应的焓变.下列说法正确的是( ) 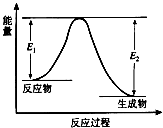
A.反应体系中加入催化剂,反应速率增大,E1减小,E2增大
B.反应体系中加入催化剂,反应速率增大,△H不变
C.△H<0,反应达到平衡时,升高温度,A的转化率增大
D.△H>0,反应达到平衡时,升高温度,A的转化率减少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一小块钠投入盛有5 mL饱和澄清石灰水的试管中,不可能观察到的现象是( )
A.钠熔成小球并在液面上到处游动
B.有气体生成
C.溶液中有银白色金属析出
D.溶液变浑浊
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】往1.0molL﹣1KI溶液中加入固体I2 , 发生反应:I2(aq)+I﹣ (aq)═I3﹣(aq)△H;I﹣的物质的量浓度c(I﹣)随温度T的变化曲线如图所示.已知反应第一次达到平衡时用时10s,则下列说法正确的是( ) 
A.该反应的△H>0
B.a、c两点对应的I﹣反应速率相等
C.b点时0~10s I﹣的平均反应速率为0.04molL﹣1s﹣1
D.d点时该反应在对应温度下处于平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业燃烧煤、石油等化石燃料释放出大量氮氧化物(NOx)、CO2、SO2等气体,严重污染空气.对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用.
(1)Ⅰ.脱硝:已知:H2的燃烧热为285.8kJmol﹣1
N2(g)+2O2(g)=2NO2(g)△H=+133kJmol﹣1
H2O(g)=H2O(l)△H=﹣44kJmol﹣1
催化剂存在下,H2还原NO2生成水蒸气和其它无毒物质的热化学方程式为
(2)Ⅱ.脱碳:向2L密闭容器中加入2mol CO2、6mol H2 , 在适当的催化剂作用下,发生反应:
CO2(g)+3H2(g)CH3OH(l)+H2O(l)
(I)①该反应自发进行的条件是(填“低温”、“高温”或“任意温度”)
②下列叙述能说明此反应达到平衡状态的是 .
a、混合气体的平均式量保持不变 b、CO2和H2的体积分数保持不变
c、CO2和H2的转化率相等 d、混合气体的密度保持不变
e、1mol CO2生成的同时有3mol H﹣H键断裂
(II)产物甲醇可以用作燃料电池,该电池是采用铂或碳化钨作为电极催化剂,在稀硫酸电解液中直接加入纯化后的甲醇,同时向一个电极通入空气.负极发生的电极反应式是
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2CO3俗名纯碱,下面是对纯碱采用不同分类法的分类,不正确的是( )
A. Na2CO3是碳酸盐 B. Na2CO3是盐
C. Na2CO3是钠盐 D. Na2CO3是碱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com