
【题目】金属钠放在水中浮在水面上,放在煤油中沉在油层下,煤油的密度是0.8gcm﹣3,推测钠的密度(gcm﹣3)( )
A. 大于1.0gcm﹣3 B. 小于0.8gcm﹣3
C. 介于0.8~1.0gcm﹣3之间 D. 不能确定
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案科目:高中化学 来源: 题型:
【题目】某兴趣小组探究SO2气体还原Fe3+的反应,他们使用的药品和装置如下图所示,下列说法不合理的是( )
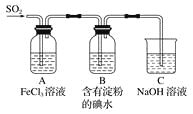
A. 能表明I-的还原性弱于SO2的现象是B中蓝色溶液褪色
B. 装置C的作用是吸收多余的SO2,防止污染空气
C. 为了验证A中发生了氧化还原反应,加入用稀盐酸酸化的BaCl2,产生白色沉淀
D. 为了验证A中发生了氧化还原反应,加入酸性KMnO4溶液,紫红色褪去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化硫是重要的化工原料,用途非常广泛。
(1)实验室用如图所示装置B制取连二亚硫酸钠(Na2S2O4)。

①实验中要控制生成SO2的速率,可采取的措施有(至少写一条)_________
②B装置中用甲醇作溶剂,C中NaOH的作用是__________。
(2)二氧化硫能够抑制细菌的滋生,可用作防腐剂,但必须严格按照国家标准使用。实验室用已知浓度的碘水来测定某粉丝样品中二氧化硫的残留量,装置如图所示。

①将粉丝样品粉碎,准确称取5.0 g,放入三颈烧瓶中,加入稀硫酸浸泡30分钟,再加适量蒸馏水,加热1小时(加热装置略去),使二氧化硫完全进入吸收装置。
②往吸收装置中加入3滴淀粉溶液作指示剂,再逐滴加入0.001 mol·L-1 I2标准溶液。
当溶液颜色__________时,恰好完全反应,写出反应的离子方程式________;恰好反应时消耗I2标准溶液10.00 mL,测得样品中SO2的残留量为________ g·kg-1。
③在配制I2标准溶液,定容加水时仰视刻度线,则测得SO2含量_______(填“偏高”“偏低”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.胶体区别于其他分散系的根本原因是胶体有丁达尔效应
B.分散系中分散质粒子直径由小到大的正确顺序是:溶液<胶体<浊液
C.向氢氧化钠溶液中边滴加饱和FeCl3溶液边振荡制备Fe(OH)3胶体
D.胶体的分散质可以通过过滤从分散剂中分离出来
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 下列现象或性质能体现钠的物理性质的是
①钠燃烧时发出黄色的火焰 ②钠燃烧时生成过氧化钠 ③熔点低 ④密度比水⑤热和电的良导体 ⑥钠有很强的还原性
A. ①③④⑤⑥ B. ①②③④⑤ C. ②③④⑤ D. ①③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列可设计成原电池的化学反应是( )
A. H2O(l)+CaO(s)=Ca(OH)2(s)
B. Ba(OH)2·8H2O+2NH4Cl=BaCl2+2NH3·H2O+8H2O
C. 2KClO3![]() 2KCl+3O2↑
2KCl+3O2↑
D. CH4(g)+2O2(g) ![]() CO2(g)+2H2O(l)
CO2(g)+2H2O(l)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验现象的叙述中,不正确的是
A. 氢气在Cl2中燃烧,产生苍白色火焰,瓶口有白雾生成
B. 铁丝在Cl2中燃烧,产生棕红色的烟
C. 钠在Cl2中燃烧,生成白色的雾
D. 铜丝在Cl2中燃烧,生成棕黄色的烟
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在2 L密闭容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如下图所示。由图中数据
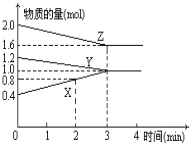
(1)该反应的化学方程式:_________________。
(2)反应开始至2 min末,X的反应速率为_______。
(3)该反应是由___________开始反应的。(填“正反应”、“逆反应”或“正、逆反应同时)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com