
| A. | 与H2SO4反应的铝粉7.2g | |
| B. | 参加反应的H2SO4为0.2mol | |
| C. | 铝与NaOH反应中消耗氧化剂约0.53mol | |
| D. | 参加反应的NaOH约为0.27mol |
分析 若铝粉在两溶液中均不足,则反应生成气体的质量之比为1:1;
若铝粉在两溶液中均过量,则生成气体的质量之比为3:2.
而现在反应完毕后生成气体的质量之比为4:3,介于1:1和3:2之间,说明铝在一种溶液中不足,在另一种溶液中过量.
根据反应方程式2Al+3H2SO4═Al2(SO4)3+3H2↑、2Al+2NaOH+2H2O═2NaAlO2+3H2↑可知,铝在NaOH溶液中不足,在硫酸中过量,据此分析.
解答 解:若铝粉在两溶液中均不足,则反应生成气体的质量之比为1:1;
若铝粉在两溶液中均过量,则生成气体的质量之比为3:2.
而现在反应完毕后生成气体的质量之比为4:3,介于1:1和3:2之间,说明铝在一种溶液中不足,在另一种溶液中过量.
根据反应方程式2Al+3H2SO4═Al2(SO4)3+3H2↑、2Al+2NaOH+2H2O═2NaAlO2+3H2↑可知,铝在NaOH溶液中不足,在硫酸中过量.
A、由于铝在氢氧化钠溶液中完全反应,而在硫酸中过量,故硫酸溶液中生成氢气的物质的量取决于硫酸,而硫酸的物质的量为0.3mol,故生成的氢气的物质的量n(H2)=0.3mol,设反应掉的铝的物质的量为xmol,则根据:2Al~3H2,可知:2Al~3H2
2 3
xmol 0.3mol
故有:$\frac{2}{xmol}=\frac{3}{0.3mol}$
解得x=0.2mol,质量m=nM=0.2mol×27g/mol=5.4g,故A错误;
B、由于硫酸完全反应,故反应掉的硫酸的物质的量为0.3mol,故B错误;
C、由于硫酸和铝反应生成氢气0.3mol,故氢氧化钠和铝反应生成氢气0.4mol,根据铝和氢氧化钠溶液反应时,水做氧化剂,且反应的原化学方程式为:2Al+2NaOH+6H2O═2NaAlO2+3H2↑+4H2O,即6H2O~3H2,设消耗的氧化剂的物质的量为ymol,则有:
6H2O~3H2
6 3
ymol 0.4mol
可知:$\frac{6}{ymol}=\frac{3}{0.4mol}$
解得y=0.8mol,故C错误;
D、由于硫酸和铝反应生成氢气0.3mol,故氢氧化钠和铝反应生成氢气0.4mol,设消耗的氢氧化钠的物质的量为zmol,根据铝和氢氧化钠溶液反应可知:
2 NaOH~3H2
2 3
zmol 0.4mol
则有:$\frac{2}{zmol}=\frac{3}{0.4mol}$
解得z≈0.27mol,故D正确.
故选D.
点评 本题考查化学反应方程式的计算,涉及过量计算问题,关键是判断反应中酸、碱是否足量,综合性较强,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 聚丙烯的结构简式为: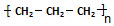 | B. | 四氯化碳分子的电子式: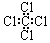 | ||
| C. | 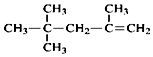 的名称为:2,4,4-三甲基-1-戊烯 的名称为:2,4,4-三甲基-1-戊烯 | D. | 乙醇分子比例模型: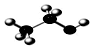 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2+、Na+、NO3-、Cl- | B. | Mg2+、NH4+、SO42-、NO3- | ||
| C. | H+、K+、Cl-、CO32- | D. | K+、Mg2+、CO32-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L水中含有NA个水分子 | |
| B. | 常温常压下,28gCO中所含的原子数目为2NA | |
| C. | 如果11.2LN2中含有n个分子,则阿伏加德罗常数一定为2n | |
| D. | 1L 1mo1/L的NaHSO4溶液中,HSO4-离子的数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na、Al、S2- | B. | Fe3+、MnO4-、NO3- | C. | Cl2、HClO、Mg | D. | O2、Cl-、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源:2016-2017学年云南省高一9月月考化学卷(解析版) 题型:选择题
下列电离方程式中,正确的是
A.Na2SO4 = 2 Na+ + SO4-2 B.Ba(OH)2 =Ba2+ +OH2-
C.H2CO3 =H+ +HCO3- D.Al2(SO4)3 =2Al3+ + 3SO42-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏卫一高一上10月月考化学a卷(解析版) 题型:选择题
实验室有三瓶失去标签的试剂,分别是Na2CO3、NaCl、AgNO3 ,实验员选择了一种试剂就把它们区别开来了,这种试剂是:
A.氯化钡溶液 B.氢氧化钠溶液 C.盐酸 D.硝酸
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
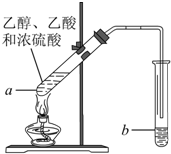 红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了有香味的酯.在实验室也可以用如图所示的装置制取乙酸乙酯,请回答下列问题.
红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了有香味的酯.在实验室也可以用如图所示的装置制取乙酸乙酯,请回答下列问题.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com