
过氧化钙是一种温和的氧化剂,常温下为白色的固体,易溶于酸,难溶于水、乙醇等溶剂。某实验小组拟选用如下装置(部分固定装置略)制备过氧化钙。
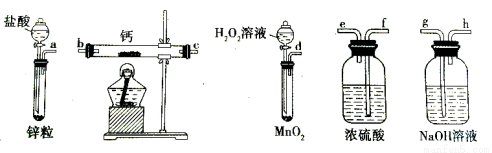
(1)请选择必要的装置,按气流方向连接顺序为 (填仪器接口的字母编号,装置可重 复使用)。
(2)根据完整的实验装置进行实验,实验步骤如下:①检验装置的气密性后,装入药品;②打开分液漏斗活塞,通入一段时间气体,加热药品;③反应结束后, (填操作);④拆除装置,取出产物。
(3)利用反应Ca2++H2O2+2NH3+8H2O=CaO2 .8H2O↓+2NH4+,在碱性环境下制取CaO2的装置如下:
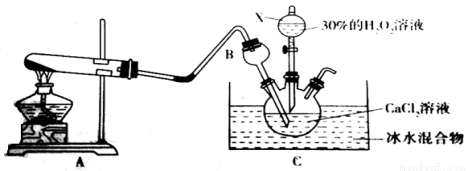
①装置A中发生反应的化学方程式为 。
②NH3在Ca2+和H2O2的反应历程中所起的作用是 。
③反应结束后,经 (填操作名称)、洗涤、低温烘干可获得CaO2 .8H2O。
检验CaO2 .8H2O是否洗涤干净的操作为 。
④已知CaO2 在350℃迅速分解生成CaO和O2。若所取产品质量是mg,加热至恒重时,
剩余固体ng,则产品中CaO2 的质量分数为 (用字母表示)。
(4)钙在空气中燃烧生成氮化钙(Ca3N2),同时可能生成过氧化钙。请利用下列试剂,设计试验检验钙的燃烧 产物中是否含有过氧化钙 。(简要说明实验步骤、现象和结论)
限选试剂:酸化的FeCl2溶液、NaOH溶液、KSCN溶液、稀硝酸
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源:2015-2016学年河北省邯郸市高二上学期第三次月考化学试卷(解析版) 题型:选择题
含有一个碳碳三键的炔烃,与氢气充分加成后的产物的结构简式为:
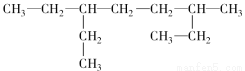 ,此炔烃可能的结构有( )
,此炔烃可能的结构有( )
A.1种 B.2种 C.3种 D.4种
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二上学期期中考试化学试卷(解析版) 题型:选择题
一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g)  2CO(g)。平衡时,体系中气体体积分数与温度的关系如图所示:已知:气体分压(P分)=气体总压(P总)×体积分数。下列说法正确的是( )
2CO(g)。平衡时,体系中气体体积分数与温度的关系如图所示:已知:气体分压(P分)=气体总压(P总)×体积分数。下列说法正确的是( )

A.550℃时,若充入惰性气体,?正,?逆 均减小,平衡不移动
B.650℃时,反应达平衡后CO2的转化率 为 25.0%
C.T℃时,若充入等体积的CO2和CO,平衡向逆反应方向移动
D.925℃时,用平衡分压代替平衡浓度表示的化学平衡常数KP=24.0P总
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省高三上学期第六次考试理综化学试卷(解析版) 题型:选择题
化学与生产、生活息息相关,下列叙述错误的是
A.浓硫酸可刻蚀石英制艺术品
B.铁表面镀锌可增强其抗腐蚀性
C.大量燃烧化石燃料是造成雾霾天气的一种重要因素
D.氢氧化铝可作胃酸的中和剂
查看答案和解析>>
科目:高中化学 来源:2016届广东省顺德市高三上第四次月考理综化学试卷(解析版) 题型:填空题
孔雀石主要含Cu2(OH)2CO3,还 含少量FeO、SiO2。以孔雀石为原料可制备CuSO4·5H2O步骤如下:
含少量FeO、SiO2。以孔雀石为原料可制备CuSO4·5H2O步骤如下:

(1)写出孔雀石与稀硫酸反应的化学方程式:___________。
(2)溶液A的金属离子有Cu2+、Fe2+。实验步骤中试剂①最佳选____(填代号)。
A.KMnO4 B.Cl2 C.H2O2 D.HNO3
(3)溶液B中加入CuO作用是______________。
(4)常温下Fe(OH)3的Ksp=1×10-39,若要将溶液中的Fe3+转化为Fe(OH)3沉淀,使溶液中c(Fe3+)降低至1×10—3mol/L,必需将溶液pH调节至____。
(5)由溶液C获得CuSO4·5H2O晶体,需要经_______、______和过滤。
(6)可用KMnO4标准溶液测定溶液A中Fe2+的浓度,量取A溶液20.00ml,用0.010mol/L酸性KMnO4标准溶液滴定,消耗KMnO4 10.00ml, A溶液中Fe2+的物质的量浓度____mol/L.(反应原理:MnO4- + 5Fe2++8H+=Mn2++5Fe3++4H2O)
查看答案和解析>>
科目:高中化学 来源:2016届安徽省高三上1月阶段测理综化学试卷(解析版) 题型:填空题
矿物燃料在使用的过程中会产生大量污染性物质,如SO2和CO2,而H2和NH3都被认为是理想的清洁能源。
(1)某些合金可用于储存氢,金属储氢的原理可表示为:M(s)+xH2═MH2x(s)△H<0(M表示某种合金)如图1表示温度分别为T1、T2时,最大吸氢量与氢气压强的关系.则下列说法中,正确的是___________;
a.T1>T2
b.增大氢气压强,加快氢气的吸收速率
c.增大M的量,上述平衡向右移动
d.上述反应可实现多次储存和释放氢气
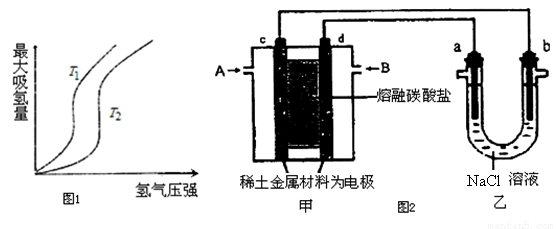
(2)以熔融碳酸盐为电解质,稀土金属材料为电极组成氢氧燃料电池(如图2装置甲所示),其中负极通入H2,正极通入O2和CO2的混合气体.图2乙装置中a、b为石墨电极,电解一段时间后,b电极附近滴入酚酞溶液变红,NaCl溶液的体积为100mL。
①工作过程中,甲装置中d电极上的电极反应式是________________;乙装置中电极a为_______极(填电极名称)。
②若在a极产生112mL(标准状况)气体,25℃时乙装置中所得溶液pH=__________。(忽略电解前后溶液的体积变化)
(3)氨在氧气中燃烧,生成水和一种空气组成成分的单质.
已知:N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ•mol-1 2H2(g)+O2(g)═2H2O(1)△H=-572KJ•mo1-1试写出氨气在氧气中燃烧生成液态水的热化学方程式________________;
(4)在一定条件下,将lmolN2和3molH2混台于一个10L的密闭容器中发生反应:
N2(g)+3H2(g) 2NH3(g)△H<0 已知5分钟后达到平衡,平衡时氨气的体积分数为25%。
2NH3(g)△H<0 已知5分钟后达到平衡,平衡时氨气的体积分数为25%。
①该反应的平衡常数表达式为:K=______________;
②能判断该反应是否达到化学平衡状态的依据是____________
a、容器中压强不变 b、混合气体的密度不变 c、3v正(H2)=2v逆(NH3) d、c(N2): c(H2): c(NH3)=1:3:2
③对于上述平衡状态,改变下列条件能使反应速率增大,且平衡向正向移动的___________
a、选用更高效的催化剂 b、升高温度 c、及时分离出氨气
d、增加H2的浓度 e、充入He,使体系总压强增大
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三上12月月考化学试卷(解析版) 题型:选择题
用下列实验装置进行相应实验,装置正确且能达到实验目的是:
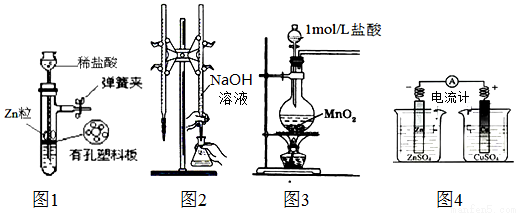
A.用图1所示装置制取少量H2
B.用图2所示装置用标准浓度的氢氧化钠溶液测定盐酸的浓度
C.用图3所示装置制取少量Cl2
D.用图4所示装置确定导线中有电流通过并确定电流方向
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高一上第二次月考化学试卷(解析版) 题型:选择题
一块表面己被缓慢氧化的金属钠,其质量为10.8g,投入100g水中,收集到氢气0.2g。则原来钠块表面被氧化的钠的质量是
A.6.2g B.4.6g C.7.8g D.10.6g
查看答案和解析>>
科目:高中化学 来源:2016届安徽省高三上第四次月考化学试卷(解析版) 题型:选择题
最近,中国科大的科学家们将C60分子组装在一个单层分子膜表面,在-268℃时冻结分子的热振荡,并利用扫描隧道显微镜首次“拍摄”到能清楚分辨碳原子间单、双键的分子图象.下列化合物分子中一定既含σ键又含π键的是
A.N2 B.CO2 C.C2H4O D.H2O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com