
【题目】T1℃时,向容积为2L的密闭容器中充入一定量的A气体和B气体,发生如下反应:A(g) +2B(g)![]() C(p)。反应过程中测定的部分数据见下表:
C(p)。反应过程中测定的部分数据见下表:
反应时间/min | n(A)/mol | n(B)/ mol |
0 | 1.00 | 1.20 |
10 | 0.50 | |
30 | 0.20 |
下列说法错误的是
A. 前10min内反应的平均速率为v(C)=0.0250 mnol·L-1·min-1
B. 保持其他条件不变,起始时向容器中充入0.50molA气体和0.60mo1B气体,到达平衡时,n(C)<0.25mo1
C. 其他条件不变时,向平衡体系中再充入0.50molA,与原平衡相比,达平衡时B的转化率增大,A的体积分数增大
D. 温度为T2℃时(T1>T2),上述反应平衡常数为20,则正反应为放热反应
【答案】D
【解析】A. 前10min内反应的平均速率为v(C)= v(A)=0.50/2/10 mnol·L-1·min-1=0.0250mnol·L-1·min-1,故A正确;B. 题干平衡时,c(C)=0.25mol/L,保持其他条件不变,起始时向容器中充入0.50molA气体和0.60mo1B气体,与题干相比相当于减压,平衡左移,达到新平衡时,n(C)<0.25mo1,故B正确;C. 其他条件不变时,向平衡体系中再充入0.50molA,与原平衡相比,达平衡时B的转化率增大,A的体积分数增大,故C正确;D. 温度为T1℃时各物质平衡浓度为:c(A)=0.25mol/L,c(B)=0.10mol/L,c(C)=0.25mol/L,平衡常数= c(C)/[ c(A) c2(B)]=100,温度为T2℃时(T1>T2),平衡常数减小,表明降温平衡左移,则正反应为吸热反应,故D错误。故选D。


科目:高中化学 来源: 题型:
【题目】正盐A、B均含三种元素,且所含元素种类相同。A在加热条件下发生如下变化。已知,气体D能使带火星的木条复燃。透过蓝色钴玻璃,A、B、C的焰色反应均为紫色。往C的溶液中加入AgNO3溶液,出现白色沉淀,再加入稀硝酸,沉淀不溶解,且沉淀质量为14.35 克。请回答:
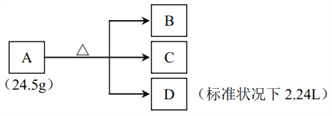
(1)C 的化学式为___________。
(2)写出 A 分解的化学方程式___________。
(3)将A与C混合,再加入稀硫酸,有气体产生,用离子方程式表示发生的反应___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中,反应2NO2(g)![]() N2O4(g),在不同条件下的化学平衡情况如图a、图b所示。图a表示恒温条件下c(NO2)的变化情况,图b表示恒压条件下,平衡体系中N2O4的质量分数随温度变化情况(实线上的任意一点为平衡状态)。下列说法正确的是
N2O4(g),在不同条件下的化学平衡情况如图a、图b所示。图a表示恒温条件下c(NO2)的变化情况,图b表示恒压条件下,平衡体系中N2O4的质量分数随温度变化情况(实线上的任意一点为平衡状态)。下列说法正确的是

图a 图b
A. 图a 中,A1→A2变化的原因一定是充入了NO2
B. 图b中,E点对应状态中,v(正)> v(逆)
C. 图b中,E→A所需的时间为x,D→C所需时间为y,则x < y
D. 依据图b分析可知,该化学反应△H>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)氯化铝水溶液呈______性 ,(填“酸”、“中”、“碱”)性,原因是(用离子方程式表示):_____________________;把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是_________。
(2)浓度均为0.1 mol/L的①硫酸 ②醋酸 ③氢氧化钠 ④氯化铵四种溶液中由水电离出的H+浓度由大到小的顺序是_________________________(填序号)。
(3)在0.5mol/L的NaHSO3溶液中滴入石蕊,溶液变红,该溶液中HSO3-的电离程度_____HSO3-的水解程度。(填“>”、“=”、“<”)
(4)常温下,将0.2 mol/L CH3COOH和0.1 mol/L NaOH溶液等体积混合,所得溶液的pH<7,该混合溶液中离子浓度由大到小的顺序是______________________________。
(5)相同浓度的下列溶液中,c(CO32-)的大小顺序是_________________(填序号)。
①Na2CO3 ②NaHCO3 ③H2CO3 ④(NH4)2CO3 ⑤NH4HCO3
(6)常温下,用0.01 mol/L HCl溶液完全中和pH=11的下列溶液各100mL,需HCl溶液体积的大小关系是_______________________________(填序号)。
①NaOH ②Ba(OH)2 ③NH3·H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2的大量排放不仅会造成温室效应还会引起海水中富含二氧化碳后酸度增加,可能会杀死一些海洋生物,甚至会溶解掉部分海床,从而造成灾难性的后果。所以二氧化碳的吸收和利用成为当前研究的重要课题。
(1)工业上以CO2与H2为原料合成甲醇,再以甲醇为原料来合成甲醚。
已知:CO2(g)+3H2(g)CH3OH(g)+H2O(g) △H1
2CH3OH(g)CH3OCH3(g)+H2O(g) △H2=-24.5 kJmol﹣1
2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g) △H3=-122.5 kJmol﹣1
甲醇的电子式为________________;△H1=________kJ·mol-1
(2)某科研小组探究用活性炭处理汽车尾气的可行性,在T1℃体积为2L的恒温密闭容器中进行了实验,并根据实验数据绘制了如下图像,其中X代表NO浓度变化,Y代表N2和CO2浓度变化:
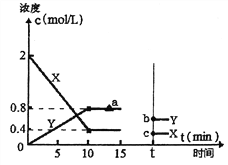
①若15min,后升高到一定温度,达到新平衡后容器中N2、CO2、NO的浓度之比为1:1:3,到达到新平衡时CO2的反应速率与图中a点相比较,速率_____(填“增大”、“减小”或“不变”),此时平衡常数K与T1℃相比_______(填“增大”、“减小”或“不变”)。②T1℃时该反应的平衡常数为_________________。
③如上图所示,若15min后改变了一个条件,t时刻建立新的平衡,b点坐标(0.6,t),c点坐标(0.3,t)。则改变的条件可能是_______(填序号)。
a.扩大容器体积 b.升高温度 c.使用合适催化剂 d.移走部分NO
(3)已知:H2CO3的电离常数Ka1=4.4×10-7,Ka2=5×10-11。25℃时若用1L 1mol· L-1的NaOH溶液吸收CO2,当溶液中c(CO32-):c(H2CO3)=2200,此时该溶液的pH值为________________。
(4)以熔融K2CO3为电解质的甲醚燃料电池,具有能量转化率高,储电量大等特点,则该电池的负极电极反应式为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A. 向MgCl2溶液中滴加过量氨水:Mg2++2OH-=Mg(OH)2↓
B. 用稀硝酸洗涤试管内壁的银镜:Ag+4H++NO![]() =Ag++NO↑+2H2O
=Ag++NO↑+2H2O
C. 将Cu粉加入到Fe2(SO4)3溶液中:2Fe3++3Cu=2Fe+3Cu2+
D. 向NaAlO2溶液中通入过量CO2:AlO![]() +CO2+2H2O=Al(OH)3↓+HCO
+CO2+2H2O=Al(OH)3↓+HCO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质用途的说法合理的是( )
A. Si可用于制造太阳能电池
B. 液氨可用作制冷剂
C. 聚氯乙烯可用于制食品包装袋
D. 漂白粉可用于杀菌消毒
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com