
科目:高中化学 来源: 题型:
| A、NaF和MgF2中阳离子与阴离子半径之比,前者小于后者 | ||||
| B、Xu+和Yu-与氖的电子层结构相同,原子半径前者大于后者 | ||||
C、
| ||||
| D、PH5和H2S的稳定性,前者大于后者 |
查看答案和解析>>
科目:高中化学 来源: 题型:022
晶胞是晶体中最小重复单位,并在空间不断伸展构成晶体。NaCl晶体是一个正六面体(如图)。我们把阴、阳离子看成不等径的圆球,并彼此相切,离子键的键长是相邻阴阳离子的半径之和(如图)。已知a为常数,请计算下列问题:
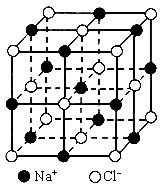
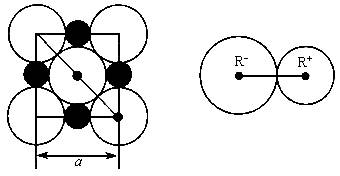
(1)每个晶胞中平均分摊________个Na+,________个Cl-;
(2)若某NaCl晶体的质量为5.85g,它约含________mol NaCl晶胞;
(3)NaCl晶体离子键的键长为________,Na+离子半径与Cl-离子半径之比为![]() ________;
________;
(4)NaCl晶体不存在分子,但在高温下(大于等于1413℃时)晶体转变成气体NaCl的分子形式存在,现有1mol NaCl晶体,加强热使其气化,测得气体体积为11.2L(已折为标准状况)。则此时氯化钠气体的分子式为________。
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:022
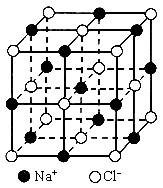
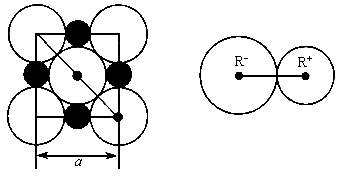
(1)每个晶胞中平均分摊________个Na+,________个Cl-;
(2)若某NaCl晶体的质量为5.85g,它约含________mol NaCl晶胞;
(3)NaCl晶体离子键的键长为________,Na+离子半径与Cl-离子半径之比为![]() ________;
________;
(4)NaCl晶体不存在分子,但在高温下(大于等于1413℃时)晶体转变成气体NaCl的分子形式存在,现有1mol NaCl晶体,加强热使其气化,测得气体体积为11.2L(已折为标准状况)。则此时氯化钠气体的分子式为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com