
【题目】下表为元素周期表中的一部分。用化学式或元素符号回答下列问题:
IA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 | |
2 | ⑥ | ⑦ | ||||||
3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
4 | ② | ④ | ⑨ |
(1)10种元素中,化学性质最不活泼的是__________(填元素名称)。
(2)三周期元素除⑩外原子半径最小的是______(填元素符号),这些元素的最高价氧化物对应水化物中碱性最强的是__________(填化学式,下同),具有两性的是____________。
(3)在室温下有颜色的气体单质溶于水的离子方程式为_____ __;
(4)⑧与⑨分别与H2形成的氢化物的稳定性:__________,(用化学式表示)最高价氧化物对应的水溶液的酸性由强到弱的顺序:______ _________。(用化学式)
(5)①③⑤单质的活泼性顺序为_____>____>____(填元素符号),判断的实验依据是__(写出一种)
【答案】(1)氩
(2)Cl KOH Al(OH)3
(3)Cl2+H2O![]() H++Cl―+HClO
H++Cl―+HClO
(4)HCl>HBr;HClO4>HBrO4
(5)Na>Mg>Al;单质分别与水或酸反应的剧烈程度(或其最高价氧化物对应的水化物的碱性强弱)合理答案即给分
【解析】试题分析:根据元素在周期表中的位置可知①~⑩分别是Na、K、Mg、Ca、Al、C、O、Cl、Br、Ar。
(1)10种元素中,化学性质最不活泼的是稀有气体元素Ar,名称为氩。
(2)同周期自左向右原子半径逐渐减小,则第三周期元素除⑩外原子半径最小的是Cl。金属性越强,最高价氧化物对应水化物的碱性越强,则这些元素的最高价氧化物对应水化物中碱性最强的是KOH,具有两性的是Al(OH)3。
(3)在室温下有颜色的气体单质是氯气,溶于水的离子方程式为Cl2+H2O![]() H++Cl―+HClO;
H++Cl―+HClO;
(4)氯元素非金属性强于溴,则⑧与⑨分别与H2形成的氢化物的稳定性为HCl>HBr;非金属性越强,最高价含氧酸的酸性越强,则最高价氧化物对应的水溶液的酸性由强到弱的顺序HClO4>HBrO4。
(5)同周期自左向右金属性逐渐减弱,则①③⑤单质的活泼性顺序为Na>Mg>Al,判断的实验依据可以是单质分别与水或酸反应的剧烈程度(或其最高价氧化物对应的水化物的碱性强弱)。


 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源: 题型:
【题目】一个碳原子上如果连有3个氢原子,则这样的氢原子称为伯氢,如果只连有2个氢原子,则这样的氢称为仲氢,例如:-CH3中的氢原子为伯氢,-CH2-中的氢原子为仲氢。已知在烷烃中伯氢和仲氢被取代的活性因反应的条件不同而不同。在高温下伯氢与仲氢被取代的活性相等,则可以称之活性比为1︰1。请回答下列问题:
(1)已知丙烷在高温下与氯气发生取代反应,反应式如下:
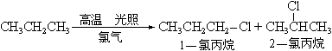
则在一氯代丙烷中1-氯丙烷在产物中的占有率为 ;
(2)常温下丙烷也能与氯气发生取代反应,反应式如下:

则在常温下伯氢和仲氢的相对活性比为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国科学家屠呦呦因青蒿素的研究荣获了2015年诺贝尔化学奖。青蒿素是继乙氨嘧啶、氯喹、伯喹之后最有效的抗疟特效药,具有速效和低毒的特点,曾被世界卫生组织称做是―世界上唯一有效的疟疾治疗药物‖。由青蒿素合成系列衍生物(它们的名称和代号如图所示)的路线如图:

回答下列问题:
(1)青蒿素的分子式为________;氢化青蒿素分子中官能团名称为______________。
(2)反应①中,有机反应类型为___________;NaBH4的作用是_______________。
A.氧化剂 B.还原剂 C.催化剂 D.溶剂
(3)有机物 D 是分子式为 C4H4O 3的五元环状化合物,请写出反应③的化学反应方程式
______________________________________________________。
(4)青蒿唬酯能够发生的反应类型有________。
A.酯化反应 B.水解反应 C.还原反应 D.加聚反应
(5)以H2Q 表示双氢青蒿素,写出反应②的化学方程式____________________________。
(6)从双氢青蒿素(H2Q)出发,可通过多步反应合成出有机物 E。合成过程中,有机原料除H2Q、![]() 外,还需含苯环的二羟基化合物F,写如有机物F与NaOH 溶液反应的离子反应方程式_____________________________________________,有机物G是F的同分异构体,有机物G遇FeCl3溶液显紫色,且有 4 种不同类型的氢,其个数比为3︰2︰2︰1,则符合条件的有机物G的同分异构体有_____种。
外,还需含苯环的二羟基化合物F,写如有机物F与NaOH 溶液反应的离子反应方程式_____________________________________________,有机物G是F的同分异构体,有机物G遇FeCl3溶液显紫色,且有 4 种不同类型的氢,其个数比为3︰2︰2︰1,则符合条件的有机物G的同分异构体有_____种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I 请回答:
(1)HClO的结构式 。
(2)明矾可用来净水,用离子方程式表示其理由 。
(3)MgCO3悬浊液经煮沸可转化为更难溶的Mg(OH)2,转化的化学方程式是 。
(4)完成以下氧化还原反应的离子方程式:
( )Fe3+ + ( )Cl2+ = ( )FeO42- + ( )Cl- +
II 盐湖提锂脱镁渣主要成分为Mg(OH)2、Li2CO3和少量CaCO3,利用盐湖提锂脱镁渣制备高纯轻质氧化镁,为盐湖镁资源综合回收利用提供了一条可行途径,生产流程如图所示:

回答下列问题:
(1)固体A的成分是 。
(2)固体A在真空、1200℃条件下与硅单质反应生成金属镁,反应的化学方程式为 。
(3)沉淀物X中存在Mg5(CO3)4(OH)2·4H2O,则盐湖提锂脱镁渣与NH4HCO3溶液反应生成Mg5(CO3)4(OH)2·4H2O的化学方程式是 。
(4)实际生产中NH4HCO3与Mg(OH)2等物质的量之比要比(3)中反应理论值大的原因是
。
(5)欲检验沉淀物X是否煅烧完全,请设计简要的实验方案:
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以煤为原料可合成涂料H(如下图)。B分子式为C2H6O,能与钠反应放出氢气。(注:流程中某些反应条件没有给出)。
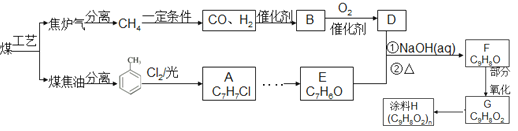
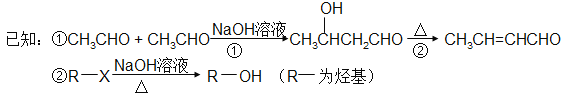
请回答:
(1)流程中煤的综合利用的工艺名称为 。
(2)B的结构简式是 ,E中含氧官能团的名称是 。
(3)G→H反应的化学方程式 。
(4)对于化合物F,下列说法正确的是 。
A、能发生银镜反应 B、能使Br2的CCl4溶液褪色
C、能发生水解反应 D、能与金属钠反应
(5)下列有机物与G不是互为同分异构体的是 。
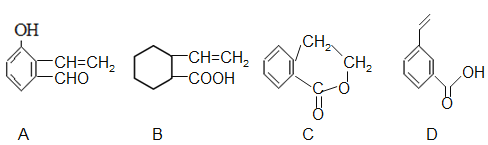
(6)从 →E 的合成路线(试剂及溶剂任选:合成路线参照“已知①”中书写形式) 。
→E 的合成路线(试剂及溶剂任选:合成路线参照“已知①”中书写形式) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】央视曝光某品牌食品在生产中使用“瘦肉精”猪肉。瘦肉精(Clenbuterol)是一种廉价药品,学名盐酸克伦特罗。它对于减少脂肪增加瘦肉作用非常好,但它有很危险的副作用,轻则导致心律不整,重则导致心脏病.盐酸克伦特罗的结构简式如图.下列有关说法错误的是

A.该有机物H-NMR谱有7个峰
B.该有机物的分子式为C12H17N2Cl2O
C.该有机物中含有2个手性碳原子
D.该有机物能发生加成反应、取代反应、氧化反应和消去反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿魏酸在食品、医药等方面有着广泛用途。一种合成阿魏酸的反应可表示为

下列说法正确的是
A. 可用酸性KMnO4溶液检测上述反应是否有阿魏酸生成
B. 香兰素、阿魏酸均可与Na2CO3、NaOH溶液反应
C. 通常条件下,香兰素、阿魏酸都能发生取代、加成、消去反应
D. 与香兰素互为同分异构体,分子中有4种不同化学环境的氢,且能发生银镜反应的酚类化合物共有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸橙花酯是一种食用香料,其结构简式如图所示,关于该有机物的下列叙述中正确的是

①分子式为C12H20O2
②能使酸性KMnO4溶液褪色
③能发生加成反应,但不能发生取代反应
④它的同分异构体中可能有芳香族化合物,且属于芳香族化合物的同分异构体有8种
⑤1mol该有机物水解时只能消耗1molNaOH
⑥1mol该有机物在一定条件下和H2反应,共消耗H2为3mol
A.①②③ B.①②⑤ C.①②⑤⑥ D.①②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以炼锌烟尘(主要成份为ZnO,含少量CuO和FeO)为原料,可以制取氯化锌和金属锌。
Ⅰ、制取氯化锌主要工艺如下:
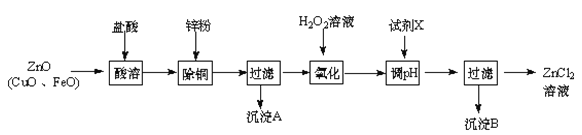
已知:Zn及化合物的性质与Al及化合物的性质相似,pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-。下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算)。

(1)加入H2O2溶液发生反应的离子方程式为 。
(2)流程图中,为了降低溶液的酸度,试剂X可以是 (选填序号:a.ZnO;b.Zn(OH)2 ;c.Zn2(OH)2CO3 ;d.ZnSO4);pH应调整到 。
(3)氯化锌能催化乳酸(![]() )生成丙交酯(C6H8O4)和聚乳酸,丙交酯的结构简式为 ,聚乳酸的结构简式为 。
)生成丙交酯(C6H8O4)和聚乳酸,丙交酯的结构简式为 ,聚乳酸的结构简式为 。
Ⅱ、制取金属锌采用碱溶解{ZnO(s)+2NaOH(aq)+H2O(l)=Na2[Zn(OH)4](aq)},然后电解浸取液。
(4)以石墨作电极电解时,阳极产生的气体为 ;阴极的电极反应为 。
(5)炼锌烟尘采用碱溶,而不采用酸溶后电解,主要原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com