
| A. | 1.0mol•L-1 | B. | 0.8mol•L-1 | C. | 0.6mol•L-1 | D. | 0.4mol•L-1 |
分析 进入溶液的是铁单质,产生的是NO,根据差量法可以计算一氧化氮的质量,金属和硝酸之间的反应分为铁过量和不足两种情况,可以根据一氧化氮的物质的量确定是哪种情况,根据电子守恒和元素守恒设未知数进行计算即可.
解答 解:铁与稀硝酸可能发生反应:Fe+4HNO3=Fe(NO3)3+NO↑+2H2O、3Fe+8HNO3=3Fe(NO3)2+2NO↑+4H2O,
由质量守恒可知m(NO)=15g-9g=6g,n(NO)=$\frac{6g}{30g/mol}$=0.2mol,
n(Fe)=$\frac{15g}{56g/mol}$=0.27mol,
若生成Fe(NO3)3,则生成0.27molNO,
如生成Fe(NO3)2,则生成0.27mol×$\frac{2}{3}$=0.18molNO,
则说明生成Fe(NO3)3和Fe(NO3)2,
令Fe(NO3)3和Fe(NO3)2物质的量分别为xmol、ymol,
根据Fe元素守恒及电子转移守恒,可得:x+y=0.27,3x+2y=0.2×3,
解得x=0.06、y=0.21,
根据N元素守恒可知,n(HNO3)=3n[Fe(NO3)3]+2n[Fe(NO3)2]+n(NO)=3×0.06mol+2×0.21mol+0.2mol=0.8mol,
原硝酸的物质的量浓度=$\frac{0.8mol}{1L}$=0.8 mol/L,
故选B.
点评 本题考查学生金属铁和硝酸之间的反应情况,明确反应产物是解题关键,注意元素守恒和电子守恒的应用是重点,难度较大.


 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案科目:高中化学 来源: 题型:填空题
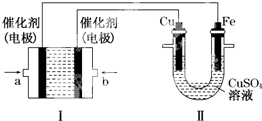
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在铁件上镀铜时,金属铜作阳极 | |
| B. | 实验室制氢气用粗锌比用纯锌速率快 | |
| C. | 电解精炼铜时,粗铜电极上每转移0.2 mol e-,阴极析出6.4 g Cu(忽略能量损失) | |
| D. | 甲醇和氧气以及KOH溶液构成的新型燃料电池中,负极反应为:CH3OH+6OH--6e-═CO2+5H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某化学小组以环己醇制备环己烯(如图1),
某化学小组以环己醇制备环己烯(如图1), $→_{85℃}^{浓H_{2}SO_{4}}$
$→_{85℃}^{浓H_{2}SO_{4}}$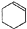 +H2O
+H2O| 密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Cu2+、Cl-、NO3- | B. | Na+、K+、SO32-、CO32- | ||
| C. | K+、HCO3-、NO3-、Cl- | D. | Ca2+、Mg2+、NO3-、Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com