
����Ŀ��ij�о���ѧϰС��������ʾװ��̽��������������ʡ���װ���й̶�����δ������
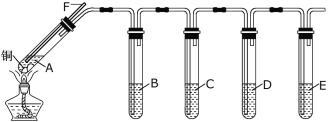
��1��A����װ�Լ�ΪͭƬ�� �������Լ����ƣ���
��2��D���Լ�Ϊ0.5 mol/L BaCl2��Һ��ʵ������������������ΪͬŨ�ȵ�Ba(NO3)2��Һ������ְ�ɫ�������˳����Ļ�ѧʽΪ ��֤��SO2���� �ԡ�
��3��װ��B������֤SO2��Ư���ԣ���������װ��Һ����Ϊ ��
A�����Ը��������Һ B��Ʒ����Һ C��ʯ����Һ D����ɫ�ĵ⡪������Һ
��4��ʵ��ʱ��B����Һ��ɫ�����д�������ð������ʼ��δ��C�б��ͳ���ʯ��ˮ���ֻ��ǻ���������Ʋ����ԭ�����ʵ����֤��
����ԭ�� ��
ʵ����֤�� ��
��5��E��Na2S��Һ������֤SO2�������ԣ�Ԥ�ڹ۲쵽������Ϊ ��
��6��ָ������װ����һ�����ԵIJ��㣺 ��
���𰸡�(1)Ũ���� ��2��BaSO4 �� ��ԭ����3��B��
��4��SO2�����Ŀ�������ܽ�Ƚϴ�Ca(OH)2�ܽ�Ⱥ�С������ʯ��ˮŨ��С������Ѹ������Ca(HSO3)2��Һ��ȡ������Ӧ��D�е���Һ�������м�������������Һ���۲��Ƿ��г������ɡ��������ȡ����������SO2����ȷ�������
��5����Һ�г��ֵ���ɫ���� ��6��ȱ��β������װ�á�
��������
�����������1����ʵ���Ŀ����̽��������������ʣ�Aװ�����Ʊ��������������װ�ã�ͭ��Ũ�����ڼ��ȵ������������ɶ�����������A����װ�Լ�ΪͭƬ��Ũ���ᡣ
��2��D���Լ�Ϊ0.5 mol/L BaCl2��Һ��ʵ��������������˵������������BaCl2����Ӧ������ΪͬŨ�ȵ�Ba(NO3)2��Һ������ְ�ɫ�������ó�����������������ᱵ���������ᱵ�Ļ�ѧʽΪBaSO4���������ᱵ��ԭ���ǣ�SO2����ˮ���������ᵼ����Һ�����ԣ��������ᱵ��Һ��H+��NO3-�ܽ������������������ᣬ�������Ȼ�����Ӧ�������ᱵ���÷�Ӧ�У�SԪ�صĻ��ϼ���+4�����ߵ�+6�ۣ�֤��SO2���л�ԭ�ԡ�
��3��SO2��ʹƷ����Һ��ɫ���÷�Ӧ���ֶ��������Ư���ԣ�����װ��B������֤SO2��Ư���ԣ���������װ��ҺΪƷ����Һ����ѡB��
��4��SO2�����Ŀ�������ܽ�Ƚϴ�Ca(OH)2�ܽ�Ⱥ�С������ʯ��ˮŨ��С������Ѹ������Ca(HSO3)2��Һ������ʵ��ʱ��B����Һ��ɫ�����д�������ð������ʼ��δ��C�б��ͳ���ʯ��ˮ���ֻ��ǻ������ʵ����֤����Ϊȡ������Ӧ��D�е���Һ�������м�������������Һ���۲��Ƿ��г������ɡ�
��5��Na2S��Һ������֤SO2�������ԣ����ݻ�ѧ��Ӧ2H2O+2Na2S+SO2=3S��+4NaOH�����Թ۲쵽������Ϊ��Һ�г��ֵ���ɫ���ǡ�
��6������װ����һ�����ԵIJ�����ȱ��β������װ�á�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. ����ϩ�����ۺ͵����ʶ�����Ȼ�߷��ӻ�����
B. ����ɷ���������Ӧ�����ܷ���ȡ����Ӧ
C. �ױ����״���������ò����һ��ȡ���ﹲ��5��
D. �ұ������е�̼ԭ�Ӳ����ܶ�����ͬ��ƽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ɫ��ѧ������Ҫ����֮һ�ǴӼ�������������ƿ��еĻ�ѧ��Ӧ��ʹԭ�ӳ�����ã���������Ⱦ����л�ѧ��Ӧ�����ϡ���ɫ��ѧ����������� ��
A���������飺CH2=CH2+HCl![]() CH3CH2Cl
CH3CH2Cl
B���Ƽ���ϩ�������CH3C��CH+CO+CH3OH ![]() CH2=C��CH3��COOCH3
CH2=C��CH3��COOCH3
C����CuSO4��2Cu+O2 = 2CuO��CuO+H2SO4��ϡ���TCuSO4+H2O
D����Cu��NO3��2��Cu+4HNO3��Ũ���TCu��NO3��2+2NO2��+2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ɫ��Ӧʵ��ʱ��ͨ������ϴ�Ӳ�˿����
A. ϡ���� B. ϡ���� C. �ռ���Һ D. ����ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������£�����ѪҺ��pH��Χ�� �� ��
A��8.67---9.26 B��7.00 C��7.35---7.45 D������5.70
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijKCl��MgCl2,��Mg(NO3)2�γɵĻ������c(K+) = 0.1mol/L ��c(Mg2+) =0.25 mol/L ��c (Cl-) = 0.2 mol/L����c(NO3-)Ϊ
A. 0.15mol/L B. 0.10mol/L C. 0.25mol/L D. 0.40mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˳�ȥMgCl2������Һ�е�Fe3+�����ڼ��Ƚ���������¼���һ���Լ����˺����ټ��������������������Լ���()
A. MgCO3 B. NaOH C. Na2CO3 D. NH3H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ڳ����·���ˮ��ʱ����Ӧ�����ӷ���ʽ��ȷ���ǣ� ��
A. Na2CO3��CO32-+2H2OH2O+CO2��+2OH-
B. NH4NO3��NH4++H2ONH3H2O+H+
C. CuSO4��Cu2++2H2OCu��OH��2��+2H+
D. KF��F-+H2O=HF+OH-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ȼ�ѧ����ʽ����H��ʾ��ȼ���ȼ���ȵ���( )
A. CO(g)��![]() O2(g)===CO2(g)����H����283 kJ��mol��1
O2(g)===CO2(g)����H����283 kJ��mol��1
B. CH4(g)��2O2(g)===CO2(g)��2H2O(g) ����H����802.3 kJ��mol��1
C. 2H2(g)��O2(g)===2H2O(l)����H����571.6 kJ��mol��1
D. 2H2(g)��O2(g)===2H2O(g)����H����484.0 kJ��mol��1
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com