
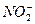 、BF3分别为直线形、V形和平面三角形。试用等电子原理说明下列分子或离子的成键情况和几何构型。
、BF3分别为直线形、V形和平面三角形。试用等电子原理说明下列分子或离子的成键情况和几何构型。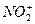 、
、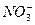 、
、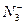 、
、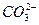
科目:高中化学 来源:不详 题型:填空题
| | | A-B | A=B | A≡B |
| CO | 键能(kJ/mol) | 357.7 | 798.9 | 1071.9 |
| 键能差值kJ/mol) | 441.2 273 | |||
| N2 | 键能(kJ/mol) | 154.8 | 418.4 | 941.7 |
| 键能差值kJ/mol) | 263.6 523.3 | |||
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.H2SO3>H2SO4? |
| B.HNO3>HNO2? |
| C.H3PO3>HPO3? |
| D.HClO>HClO4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.同主族金属的原子半径越大,金属的熔、沸点越高 |
| B.稀有气体原子序数越大,单质沸点越高 |
| C.分子间作用力越弱,分子晶体的熔点越低 |
| D.同周期元素的原子半径越小,原子越易失去电子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.能使品红试液褪色的气体不一定是SO2 |
B.胶黏剂UF结构为: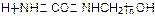 ,可推测其单体为尿素和甲醇 ,可推测其单体为尿素和甲醇 |
C.CO2电子式为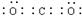 |
D.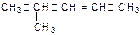 命名为4-甲基-2-戊烯 命名为4-甲基-2-戊烯 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
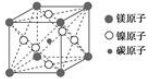
| A.Mg2CNi3 | B.MgCNi3 | C.MgCNi2 | D.MgC2Ni |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com