
分析 (1)复分解反应是两种化合物中的阴阳离子之间交换成分的反应;酸碱中和反应属于放热反应;
(2)铵盐和氢氧化钡晶体之间的反应是吸热反应;
(3)自发地氧化还原反应可以设计成原电池;
(4)物质的燃烧反应可以设计成原电池;
(5)Ba(OH)2•8H2O与NH4Cl的反应方程式为Ba(OH)2•8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O;金属铜和硝酸银之间发生置换反应得到金属铜和硝酸银.
解答 解:(1)氢氧化钠与硫酸之间的反应属于复分解反应,也是中和反应,也是放热的,故答案为:①;
(2)八水合氢氧化钡与氯化铵之间的反应是吸热反应,故答案为:③;
(3)②一氧化碳与氧气的燃烧反应可以设计成燃料电池,金属铜与硝酸银间发生置换反应得到金属铜和硝酸银,属自发的氧化还原反应,可以设计成原电池,故答案为:②④;
(4)一氧化碳与氧气的燃烧反应可以设计成燃料电池,故答案为:②;
(5)八水合氢氧化钡与氯化铵的反应是吸热反应,化学方程式为Ba(OH)2•8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O;
金属铜和硝酸银之间发生置换反应得到金属铜和硝酸银,即Cu+2Ag+═Cu2++2Ag,故答案为:Ba(OH)2•8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O;Cu+2Ag+═Cu2++2Ag.
点评 本题考查学生复分解反应、置换反应类型的特点、原电池的构成条件以及反应式的书写等方面的知识,属于综合知识的考查,难度中等.


科目:高中化学 来源: 题型:解答题
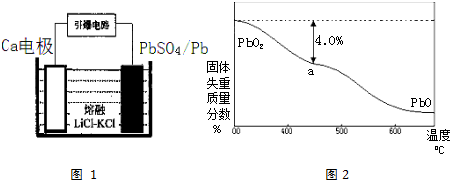
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | 实验方案 | 实验现象 |
| ① | 向盛有少量溴化钠溶液的试管中滴加少量新制氯水,振荡,再加入少量四氯化碳,振荡后静置 | 液体分为两层,下层 呈橙红色 |
| ② | 向盛有少量碘化钠溶液的试管中滴加少量新制溴水,振荡,再加入少量四氯化碳,振荡后静置 | 液体分为两层,下层 呈紫红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
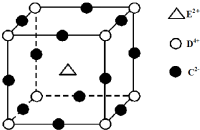 周期表中前四周期元素A、B、C、D、E的原子序数依次增大.元素A的单质有多种同素异形体,其中一种是天然存在的最坚硬的固体;元素C的原子最外层电子数是其内层的3倍;基态D原子的价电子排布为(n+1)dn(n+2)sn;基态E2+的3d轨道中有5个电子.
周期表中前四周期元素A、B、C、D、E的原子序数依次增大.元素A的单质有多种同素异形体,其中一种是天然存在的最坚硬的固体;元素C的原子最外层电子数是其内层的3倍;基态D原子的价电子排布为(n+1)dn(n+2)sn;基态E2+的3d轨道中有5个电子.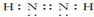 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com