
| A. | 乙烷与氯气制备一氯乙烷 | |
| B. | 在FeBr3催化作用下,苯与液溴反应制取溴苯 | |
| C. | 苯和硝酸反应制备硝基苯 | |
| D. | 乙烯与氧气在银催化作用下生成环氧乙烷 |
分析 反应符合绿色化学原子经济性要求,则反应物必须全部转化为生成物,可为加成反应,且没有气体副产品生成,以此解答该题.
解答 解:A.乙烷与氯气制备一氯乙烷为取代反应,有副产品HCl、二氯乙烷、三氯乙烷等生成,故A错误;
B.在FeBr3催化作用下,苯与液溴反应制取溴苯,同时生成HBr,故B错误;
C.苯和硝酸反应制备硝基苯,有副产品H2O生成,故C错误;
D.乙烯与氧气在银的催化作用下生成环氧乙烷,反应物全部转化为环氧乙烷从理论、经济、环保及操作等方面都很好,符合绿色化学思想,故D正确.
故选D.
点评 本题考查有机物的结构和性质,侧重于化学与生活、生产的考查,有利于培养学生良好的科学素养,提高学习的积极性,题目涉及绿色化学,明确实质是反应物全部反应生成所需的产物,不造成浪费、污染,根据题目信息解答.


科目:高中化学 来源: 题型:解答题
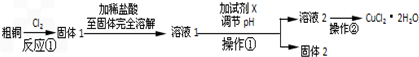
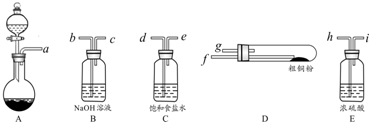
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X、Y两种元素可能能形成多种化合物 | |
| B. | X、Y中X的氢化物的稳定性强 | |
| C. | 氧化物能和氢氧化钠反应的元素可能有4种 | |
| D. | 元素W的某些化合物可作为水处理剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KHCO3═K++H++CO32- | B. | NaHSO4═Na++H++SO42- | ||
| C. | KClO3═K++ClO3- | D. | Ba(OH)2═Ba2++2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
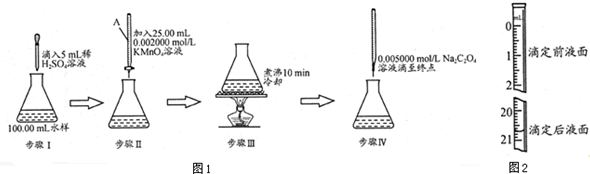
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3517Cl、3717Cl为不同核素,其化学性质不同 | |
| B. | 元素的相对原子质量,是按照该元素各种核素原子所占的一定百分比算出的平均值 | |
| C. | 目前已发现的所有元素占据了周期表里全部位置,不可能再有新的元素发现 | |
| D. | 常温常压下,非金属元素的原子都能形成气态单质分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com