
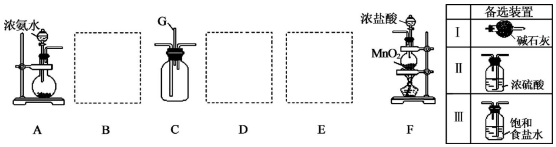
分析 (1)浓盐酸和二氧化锰在加热条件下反应生成氯化锰、氯气和水,注意稀盐酸和二氧化锰不反应;
(2)利用物质溶解时放出的热量促进氨水的挥发来制取氨气,且该物质和氨气不反应;
(3)根据杂质的性质选择除杂装置,氨气是碱性气体,要除去水蒸气只能用碱性物质,制得的氯气中混有氯化氢气体和水蒸气,因用饱和的氯化钠溶液和浓硫酸除去;
(4)根据化学反应前后元素守恒来书写方程式;
解答 解:(1)浓盐酸和二氧化锰在加热条件下反应生成氯化锰、氯气和水,离子反应为MnO2+4H++2C1-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++C12↑+2H2O,
故答案为:MnO2+4H++2C1-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++C12↑+2H2O
(2)利用物质溶解时放出的热量促进氨水的挥发来制取氨气,且该物质和氨气不反应,氨气是碱性气体,所以溶解的物质必须是碱性物质,A.碱石灰、B.生石灰都是碱性物质,且溶解于水时放出热量,C、二氧化硅不溶于水,D.五氧化二磷虽然溶于水时放热,但是酸性物质.
故选A、B
故答案为:AB
(3)氨气中混有水蒸气,氨气是碱性气体,要除去水蒸气只能用碱性物质,故B选Ⅰ;制取的氯气中混有氯化氢气体和水蒸气,氯化氢极易溶于水,氯气也能溶于水,所以不能用水除去氯化氢气体;氯气和水反应生成盐酸和次氯酸,食盐水中含有氯离子,能抑制氯气的溶解,所以要想除去氯气中的氯化氢E应选Ⅲ;水蒸气常用浓硫酸除去,故D选Ⅱ.
故答案为:Ⅰ;Ⅱ;Ⅲ;
(4)因为根据化学反应前后元素守恒且NH3和NO生成两种对环境无害的物质故方程式为4NH3+6NO=5N2+6H2O ~12mole-
~12mole-
5mol 12mol
0.5mol 1.2mol
故答案为:4NH3+6NO=5N2+6H2O;1.2mol
点评 本提考查了氨气、氯气的制备和二者性质的检验,熟悉制备原理、各仪器的作用是解题关键,注意氨根离子检验方法,为高频考点,题目难度中等.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
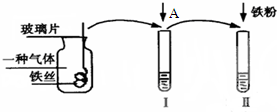 如图是某次实验探究铁及其化合物性质的流程图:
如图是某次实验探究铁及其化合物性质的流程图:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可在分液漏斗内用四氯化碳萃取碘酒中的碘单质 | |
| B. | 放出下层液体时,应打开上方的玻璃塞,并使下端管口紧贴烧杯内壁 | |
| C. | 在分液漏斗中加入萃取剂后应上下颠倒摇匀使萃取剂与溶质充分接触 | |
| D. | 分液漏斗在使用前只需检查旋塞芯处是否漏水即可 |
查看答案和解析>>
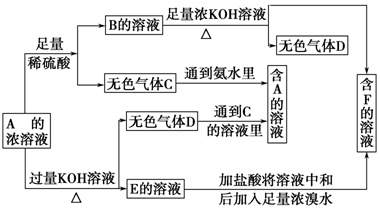
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c=$\frac{b}{11.2V}$ | B. | p=m+$\frac{{V}_{c}}{125}$ | C. | n=m+17Vc | D. | $\frac{17}{9}$m<p<$\frac{5}{3}$m |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com