
| n |
| V |
| 8g |
| 40g/mol |
| 500mL |
| 1000mL |
| 0.1mol |
| 0.1L |


科目:高中化学 来源: 题型:
| A、1,3-丁二烯和2-丁炔稳定性的相对大小 |
| B、1,3-丁二烯和2-丁炔分子储存能量的相对高低 |
| C、1,3-丁二烯和2-丁炔相互转化的热效应 |
| D、一个碳碳叁键的键能与两个碳碳双键的键能之和的大小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙醇、乙烯都可被酸性高锰酸钾溶液氧化 |
| B、乙烯、苯都可与溴水发生加成反应 |
| C、乙醇、乙酸都可以发生酯化反应 |
| D、淀粉、油脂都可以发生水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
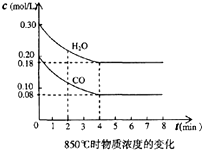 在体积为10L的容器中,通人一定量的CO和H2O,在850℃时发生如下反应:
在体积为10L的容器中,通人一定量的CO和H2O,在850℃时发生如下反应:查看答案和解析>>
科目:高中化学 来源: 题型:
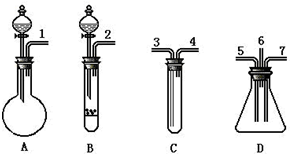 根据下面提供的仪器和试剂,完成验证SO2既有氧化性又有还原性的实验.可选用的仪器如图所示:
根据下面提供的仪器和试剂,完成验证SO2既有氧化性又有还原性的实验.可选用的仪器如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:
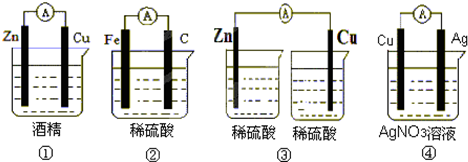
查看答案和解析>>
科目:高中化学 来源: 题型:
A Z |
查看答案和解析>>
科目:高中化学 来源: 题型:
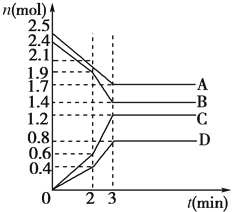 在某一容积为2L的密闭容器中,A、B、C、D四种气体物质的量(n)随时间(t)的变化曲线如图所示:
在某一容积为2L的密闭容器中,A、B、C、D四种气体物质的量(n)随时间(t)的变化曲线如图所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com