

分析 (1)①P4(s,白磷)+5O2(g)=P4O10(s)△H1=-2983.2kJ/mol(I),
P(s,红磷)+$\frac{5}{4}$O2(g)=$\frac{1}{4}$P4O10(s)△H2=-738.5kJ/mol(Ⅱ)
由盖斯定律可知(I)-(Ⅱ)×4可得:P4(s,白磷)=4P(s,红磷);
②焓变等于反应物转化键能之和减去生成物中键能之和;
(2)①燃烧热是1mol可燃物完全燃烧生成稳定的氧化物放出的热量,且物质的量与热量成正比;
②由H2和C3H8的燃烧热,结合物质的量与热量成正比计算.
解答 解:(1)P4(s,白磷)+5O2(g)=P4O10(s)△H1=-2983.2kJ/mol(I),
P(s,红磷)+$\frac{5}{4}$O2(g)=$\frac{1}{4}$P4O10(s)△H2=-738.5kJ/mol(Ⅱ)
由盖斯定律可知(I)-(Ⅱ)×4可得:P4(s,白磷)=4P(s,红磷),则△H=(-2983.2kJ/mol)-(-738.5kJ)×4=-29.2kJ/mol;
即热化学方程式为:P4(s,白磷)=4P(s,红磷)△H=-29.2kJ/mol;
故答案为:P4(s,白磷)=4P(s,红磷)△H=-29.2kJ/mol;
②已知白磷和PCl3的分子结构如图所示,由提供以下化学键的键能(kJ•mol-1):P-P 198,Cl-Cl 243,P-Cl 331.则反应P4(白磷,s)+6Cl2(g)═4PCl3(s)的反应热△H=198kJ/mol×6+6×243kJ/mol-4×3×331kJ/mol=-1326kJ/mol;
故答案为:-1326kJ/mol;
(2)①燃烧热是1mol可燃物完全燃烧生成稳定的氧化物放出的热量,由2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ/mol,则1mol氢气完全燃烧生成液态水放出的热量为285.8kJ,则氢气的燃烧热为△H=-285.8kJ/mol,
故答案为:-285.8kJ/mol;
②由氢气的燃烧热为△H=-285.8kJ/mol,丙烷燃烧热△H=-2220kJ/mol,可知1mol 氢气和0.5mol丙烷的混合气完全燃烧时放热为285.8kJ/mol×1mol+2220kJ/mol×0.5mol=1395.8kJ,
故答案为:1395.8kJ.
点评 本题考查反应热与焓变,为高频考点,把握盖斯定律应用、焓变与键能的关系为解答的关键,侧重分析与应用能力的考查,注意盖斯定律及燃烧热的判断,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | ①④⑤⑥⑦ | B. | ①③④⑤ | C. | ②④⑤ | D. | ①②⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
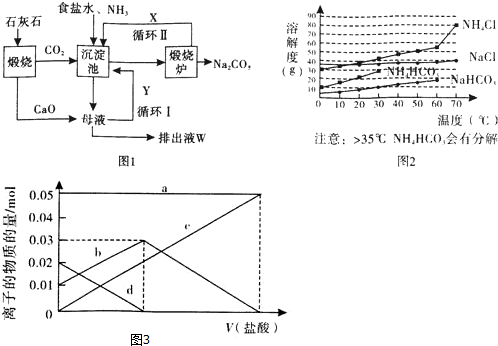
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
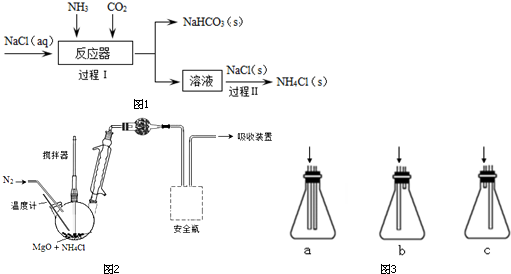
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
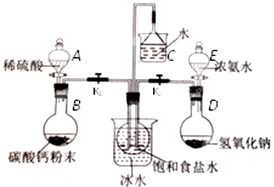
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
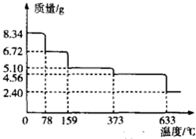 铁及其化合物在工农业生产、科学研究等方面具有广泛用途.回答下列问题:
铁及其化合物在工农业生产、科学研究等方面具有广泛用途.回答下列问题:| 温度/℃ | 500 | 700 | 900 |
| K | 1.00 | x | Y |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
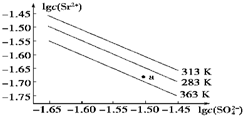
| A. | 温度一定时,Ksp(SrSO4)随c(SO42- )的增大而减小 | |
| B. | 三个不同温度中,313 K时Ksp(SrSO4)最大 | |
| C. | 283 K时,图中a点对应的溶液是饱和溶液 | |
| D. | 283 K下的SrSO4饱和溶液升温到363 K后变为不饱和溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 发生化学反应时失去电子越多的金属原子,还原能力越强 | |
| B. | NaCl只有在水溶液中才能电离出Na+、Cl- | |
| C. | 能与酸反应的氧化物,不一定是碱性氧化物 | |
| D. | 电离时能产生H+的化合物是酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com