
����Ŀ���Ժ�Fe2O3��FeO��SiO2��Al2O3�Ļ����Ϊԭ�ϣ���������Ʊ����죨Fe2O3���ķ��������ֲ�������ȥ�� [����1]![]()
[����2]![]()
��1����ҺA�������������� ��
��2������˫��ˮ�������� ��
��3������C�ijɷ������ѧʽ����
��4���Լ�x����ѡ��������ţ��� a��NaOH��Һ b����ˮ c��������̼ d��ϡH2SO4
��5�����Լ�x��ȡԭ�Ϸ��������ӷ���ʽ���� ��
���𰸡�
��1��Fe3+��Fe2+��Al3+����H+��
��2����Fe2+ȫ��ת��ΪFe3+
��3��Fe��OH��3
��4��a
��5��SiO2+2OH��=SiO32��+H2O�� Al2O3+2OH��=2AlO2��+H2O
���������⣺��1����Fe2O3��FeO��SiO2��Al2O3�Ļ����Ϊԭ�ϼ������ܽ⣬��ҺA��������������Fe3+��Fe2+��Al3+����H+����
���Դ��ǣ�Fe3+��Fe2+��Al3+����H+������2����ҺA��H2O2������������Fe2+ ȫ��ת��ΪFe3+��
���Դ��ǣ���Fe2+ ȫ��ת��ΪFe3+����3������������Fe3+��Al3+����Һ�м����������������ƣ���Ӧ����Fe��OH��3��NaAlO2������C�ijɷ���Fe��OH��3��
���Դ��ǣ�Fe��OH��3����4���Լ�x����ѡ���������ƣ�
���Դ��ǣ�a����5�����Լ�x���������ƣ���ȡԭ�Ϸ��������ӷ���ʽ�ǣ�SiO2+2OH��=SiO32��+H2O��Al2O3+2OH��=2AlO2��+H2O��
���Դ��ǣ�SiO2+2OH��=SiO32��+H2O��Al2O3+2OH��=2AlO2��+H2O��


 ���ʿ��ÿ��ֳɳ�ϵ�д�
���ʿ��ÿ��ֳɳ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ��һԪǿ��MOH��Һ�м���һ����HA��Ӧ֮����Һ�����ԣ������ж���ȷ����(����)
A.����������
B.���ǰ���������������ʵ������
C.���ɵ��β�����ˮ��
D.��Ӧ����Һ�е�A����M�����ʵ���Ũ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о����ÿ��һ��ƻ��,ҽ��Զ���ҡ�,˵��ƻ����һ�ֶ����彡���dz������ˮ��,ƻ��Ϊ�����ṩ����ҪӪ������( )
A.��֬
B.����
C.������
D.����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�л���B�Ƿ������ĺ������������Է�������������120��B�к�������������Ϊ14.8%��B��NaOH��Һ��������Ӧ���л���A��һ�������¿ɷ�����ӦA+H2O ![]() B+C���й�C��ת����ϵ��ͼ��ʾ��
B+C���й�C��ת����ϵ��ͼ��ʾ�� 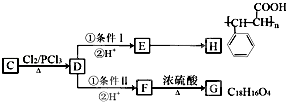
��֪�� ![]()
����������Ϣ���ش��������⣺
��1��B�Ľṹ��ʽΪ �� �������о���Ҫ���Լ�Ϊ ��
��2���й�C��ת����ϵͼ���������ķ�Ӧ������ȡ����Ӧ��������
��3��C��ͬ���칹���У�ͬʱ��������Ҫ����������֣� a������������������ b���ܷ���������Ӧ c���ܷ�����ȥ��Ӧ
��4��д������ת���Ļ�ѧ����ʽ��F��E��F��G ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ࡱ��ʵ���������30%�Ĺ���������Һ�м��������������̺ͱ�����Լ���������ͼ�� 
��1����Ҫ��Ӧ�Ļ�ѧ����ʽ�� ��
��2���������ⱻ��Ϊ��ɫ��������ԭ����������ţ��� a�������������ǿ������
b����������Ļ�ԭ������ˮ
c�������Ĺ������������зֽ�
��3����ȡ��������Ĺ�����ͼ�� ![]()
������������ȡ���������ķ�Ӧ������Ӧ������ţ���
a������ b���ֽ� c��������ԭ
���ù���������ȡ��������Ļ�ѧ����ʽ�� ��
��4�����ؾ�ʯΪԭ����ȡ�������⣬�ƵõĹ�������Ũ�ȵ����ܺĸߣ��������������ȡ��������ķ�������ԭ���Ϸ�����������������ţ��� a����һ�������£�O2����H2O
b����һ�������£�H2��ԭH2O
c����һ�������£�O2����H2 ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����в��ֶ�����Ԫ�ص����ʻ�ԭ�ӽṹ���±���
Ԫ�� | Ԫ�����ʻ�ԭ�ӵĽṹ |
T | 2p����ܼ���������s�ܼ���������1�� |
X | L��p�ܼ���������s�ܼ���������2�� |
Y | ��������Ԫ�صļ������а뾶��С |
Z | L����3��δ�ɶԵ��� |
��1��д��Ԫ��X�����ӽṹʾ��ͼ�� �� д��Ԫ��Z�ļ���̬�⻯��ĵ���ʽ��
��2��д��Ԫ��Y������������Ӧ��ˮ������KOH��Ӧ�Ļ�ѧ����ʽ�� ��
��3��T��Y��Z����Ԫ�صĵ����л�ѧ�������Բ�ͬ���������ʵ�������Ԫ�ط��ţ���ͬ����Ԫ��T���Ȼ�����ȣ��ǽ����Խ�ǿ���� �� ���б�������֤����һ��ʵ����������ĸ����
a����������������ɫ��T���ʵ���ɫ��
b��T�ĵ���ͨ���Ȼ���ˮ��Һ�в����û�����
c������T�γɻ������У���Ԫ�س����ۣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ȼ�����S2Cl2���ǹ㷺������ҵ��������������һ�ֳȻ�ɫ�ж����Һ�壬���ķ��ӽṹ��ͼ��ʾ�� 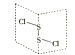
��1��S2Cl2�ĽṹʽΪ �� �仯ѧ��������������Լ������Ǽ��Լ������Լ��ͷǼ��Լ�������
��2���縺�ԣ�S�������������Cl��S2Cl2����Ļ��ϼ�Ϊ ��
��3��S2Cl2������Sԭ�ӵ��ӻ��������Ϊ �� ÿ��Sԭ�����Ի����Ӷԣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʵ�����ʵ����������ж���ȷ���ǣ������� 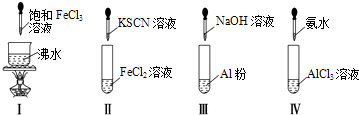
A.ʵ��������ɫ����
B.ʵ�����Һ��ɫ���
C.ʵ��ų���������
D.ʵ������ȳ��ְ�ɫ���������ܽ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com