
| 1 |
| 6 |
| A、N2 |
| B、NO |
| C、N2O |
| D、NH4NO3 |
| 1 |
| 6 |
| 1 |
| 6 |


 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、需要加热才能发生的反应一定是吸热反应 |
| B、CO(g)的燃烧热是283.0 kJ?mol-1,则2CO2(g)=2CO(g)+O2(g)反应的△H=+566.0 kJ?mol-1 |
| C、1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷燃烧热 |
| D、HCl和NaOH反应的中和热△H=-57.3 kJ?mol-1,则H2SO4和Ca(OH)2反应的中和热△H=-114.6kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、10 mL pH=12的氢氧化钠溶液中加入pH=2的HA溶液至pH刚好等于7,则所得溶液体积V(总)=20 mL |
| B、Na2CO3溶液中,2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
| C、NaB溶液的pH=8,c(Na+)-c(B-)=9.9×10-7 mol/L |
| D、pH相等的①NH4NO3、②(NH4)2SO4、③NH4HSO4三种溶液中,c(NH4+)大小顺序为:①>②>③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
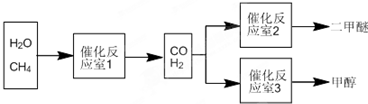
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol?L-1) | 0.44 | 0.6 | 0.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、若断开K1关闭K2,X、Y均为石墨,Z是NaCl溶液,则X 附近能得到氢氧化钠 |
| B、若断开K1关闭K2,X是纯铜,Y是粗铜,Z是CuSO4溶液,则该装置可用于铜的精炼 |
| C、若断开K2关闭K1,X是Cu,Y是Fe,Z是含有空气的海水,则该装置可用于保护Fe |
| D、若断开K2关闭K1,X是Cu,Y是Zn,Z是稀H2SO4,则在X极有气泡生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AlON和石英的化学键类型相同 |
| B、AlON和石英晶体类型相同 |
| C、AlON和(工业上通过电解法制备铝用的)Al2O3的化学键类型不同 |
| D、AlON和(工业上通过电解法制备铝用的)Al2O3晶体类型相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NA个Fe(OH)3胶体粒子的质量为107g |
| B、标准状况下,将2.24 L SO2溶于水中,溶液中H2SO3分子的数目是0.1NA |
| C、4.6 gN2O4和NO2的混合气体中含有的氧原子数为0.2NA |
| D、在含有2molH2SO4的浓硫酸中加入足量Zn粉,反应后转移的电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、人体补充必需微量元素的最好方式是食用含微量元素添加剂的食品 |
| B、碳、氢、氧、氮、磷、氯、钠、钾等都是人体必需的常量元素 |
| C、青少年在生长发育阶段要注意补钙 |
| D、碘是公认的“智慧元素”,缺碘时易患甲状腺肿大病 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com