
| 试剂 | 离子方程式 | |
| ①NaCl (Na2SO4) | ||
| ②NaCl(MgCl2) | ||
| ③NaCl(Na2CO3) |
分析 ①硫酸钡与氯化钡反应生成硫酸钡和NaCl;
②氯化镁与NaOH反应生成沉淀和氯化钠;
③碳酸钠与盐酸反应生成氯化钠,以此来解答.
解答 解:①硫酸钡与氯化钡反应生成硫酸钡和NaCl,试剂为BaCl2溶液,离子反应为Ba2++SO42-=BaSO4↓;
②氯化镁与NaOH反应生成沉淀和氯化钠,试剂为NaOH溶液,离子反应为Mg2++2OH-=Mg(OH)2↓;
③碳酸钠与盐酸反应生成氯化钠,试剂为稀盐酸,离子反应为2H++CO32-=CO2↑+H2O,
故答案为:
| 试剂 | 化学方程式 | |
| NaCl (Na2SO4) | BaCl2溶液 | Ba2++SO42-=BaSO4↓ |
| NaCl(MgCl2) | NaOH溶液 | Mg2++2OH-=Mg(OH)2↓ |
| NaCl(Na2CO3) | 稀盐酸 | 2H++CO32-=CO2↑+H2O |
点评 本题考查混合物分离提纯,侧重于学生的分析能力的考查,为高考常见题型,注意物质的性质、发生的反应为解答该类题目的关键,注意元素化合物知识的综合应用,题目难度不大.


科目:高中化学 来源: 题型:解答题
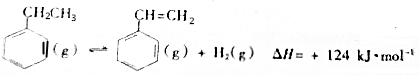
| 化学键 | C-H | C-C | C=C | H-H |
| 键能/kJ•molˉ1 | 412 | 348 | x | 436 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素 | X | Y | Z | R | T |
| 原子半径/nm | 0.037 | 0.077 | 0.074 | 0.186 | 0.102 |
| 主要化合价 | +1 | +4、-4 | -2 | +1 | +6、-2 |
| A. | X、Y、Z 位于同一周期 | |
| B. | R 与 Z 所形成的化合物均只含离子键 | |
| C. | 氢化物的沸点:Y<Z<T | |
| D. | 第一电离能:Y<Z |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A | 向盐酸酸化的Ba(NO3)2溶液中通入SO2 | 有白色沉淀生成 | BaSO3难溶于酸 |
| B | 向等浓度的KCl、Kl混合液中滴加AgNO3溶液 | 先出现白色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| C | 溴乙烷与NaOH水溶液共热后,加HNO3酸化,滴加AgNO3溶液 | 出现淡黄色沉淀 | 溴乙烷含溴元素 |
| D | 取久置的Na2O2粉末,向其中滴加过量的盐酸 | 产生无色气体 | Na2O2没有变质 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
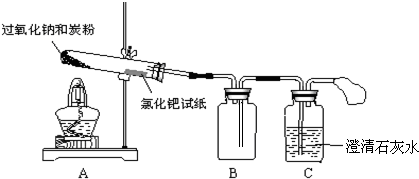
| 实验方案(不要求写具体操作过程) | 预期实验结果和结论 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
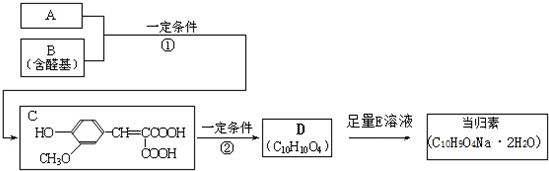
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该元素的单质性质活泼,具有较强的还原性,可以用于某些金属冶炼 | |
| B. | 该元素的单质常温下不与浓硫酸反应 | |
| C. | 该元素的单质无需特别保存,因为其性质稳定,不易与空气成分反应 | |
| D. | 该元素的最高价氧化物对应的水化物只能与酸反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Na2S和HCl | B. | Na2S和H2SO4 | C. | Na2SO3和HCl | D. | Na2SO3和H2SO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com