
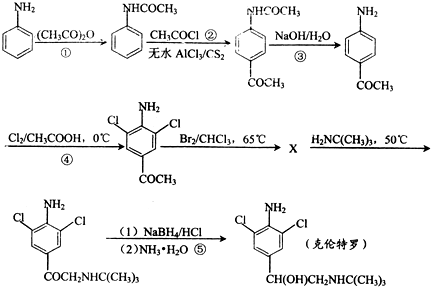
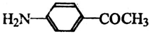
 ) 的同分异构体有多种,请写出符合以下条件的其中任意一种
) 的同分异构体有多种,请写出符合以下条件的其中任意一种 ) 的同分异构体符合以下条件:a.苯环与氨基相连,b.与新制的Cu(OH)2悬浊液加热,有红色物质生成,含有-CHO,c.苯环上有2个取代基,除去氨基外,另外的取代基为-CH2CHO;
) 的同分异构体符合以下条件:a.苯环与氨基相连,b.与新制的Cu(OH)2悬浊液加热,有红色物质生成,含有-CHO,c.苯环上有2个取代基,除去氨基外,另外的取代基为-CH2CHO; ,
, ;
; ,故答案为:
,故答案为: ;
; ) 的同分异构体符合以下条件:a.苯环与氨基相连,b.与新制的Cu(OH)2悬浊液加热,有红色物质生成,含有-CHO,c.苯环上有2个取代基,除去氨基外,另外的取代基为-CH2CHO,其中一种为
) 的同分异构体符合以下条件:a.苯环与氨基相连,b.与新制的Cu(OH)2悬浊液加热,有红色物质生成,含有-CHO,c.苯环上有2个取代基,除去氨基外,另外的取代基为-CH2CHO,其中一种为 ,故答案为:
,故答案为: ;
;

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
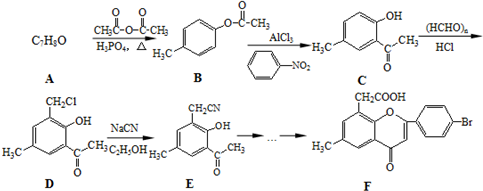
| H2O.H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HCO3-在水溶液中只电离,不水解 |
| B、硝酸钠溶液水解之后呈中性 |
| C、可溶性的铝盐都能发生水解反应 |
| D、可溶性的钾盐都不能发生水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com