
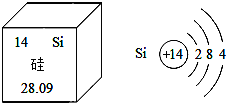
 从图中得到的正确信息是
从图中得到的正确信息是

 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
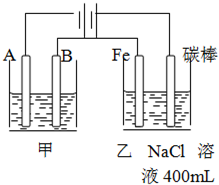 如图为相互串联的甲乙两个电解池,请回答:
如图为相互串联的甲乙两个电解池,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:
| t/min | 0 | 1 | 2 | 3 | 4 |
| n[N2O5(g)]/mol | 1.00 | 0.80 | 0.64 | a | 0.5 |
| n[NO2(g)]/mol | 0.00 | 0.40 | b | 1 | 1 |
| n[X(g)]/mol | 0.00 | 0.10 | 0.18 | 0.25 | c |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 CrO2Cl2在有机合成中可作氧化剂或氯化剂,能与许多有机物反应,可用重铬酸钾与四氯化碳反应制备:
CrO2Cl2在有机合成中可作氧化剂或氯化剂,能与许多有机物反应,可用重铬酸钾与四氯化碳反应制备:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com