
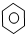
 ③CH3CH2Cl ④CH3COOH ⑤聚乙烯五种物质中:
③CH3CH2Cl ④CH3COOH ⑤聚乙烯五种物质中:分析 (1)相对分子质量在10000以上的分子为高分子;
(2)含有碳碳不饱和键的有机物能使Br2的CCl4溶液褪色;
(3)这几种物质中苯环能发生取代反应和加成反应;碳碳双键能发生加成反应、加聚反应;羧基能发生取代反应、酯化反应、中和反应;卤代烃能发生取代反应(或水解反应)、消去反应;
(4)连接醇羟基或卤原子的碳原子相邻碳原子上含有氢原子的有机物能发生取代反应、消去反应;
(5)食醋的主要成分是乙酸.
解答 解:(1)相对分子质量在10000以上的分子为高分子,这几种物质中属于高分子化合物的为,其余为小分子化合物⑤,故答案为:⑤;
(2)含有碳碳不饱和键的有机物能使Br2的CCl4溶液褪色,这几种物质只有乙烯含有碳碳不饱和键,则只有乙烯能和溴发生加成反应而使溴的四氯化碳褪色,故答案为:①;
(3)这几种物质中苯环能发生取代反应和加成反应;碳碳双键能发生加成反应、加聚反应;羧基能发生取代反应、酯化反应、中和反应;卤代烃能发生取代反应(或水解反应)、消去反应,则几种物质中只有苯能发生加成反应和取代反应,故答案为:②;
(4)连接醇羟基或卤原子的碳原子相邻碳原子上含有氢原子的有机物能发生取代反应、消去反应,则这几种物质中只有氯乙烷能发生取代反应和消去反应,故答案为:③;
(5)食醋是乙酸的水溶液,则食醋的主要成分是乙酸,故答案为:④.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系、基本概念是解本题关键,知道常见官能团及其性质,注意:并不是所有的卤代烃或醇都能发生消去反应,只有连接醇羟基或卤原子的碳原子相邻碳原子上含有氢原子的醇、卤代烃才能发生消去反应,侧重考查学生分析判断及知识灵活运用能力.


 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:高中化学 来源: 题型:选择题
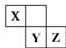 X、Y、Z 三种短周期元素在周期表中的位置如右图,X 通过共用三对电子形成 X2分子,下列说法不正确的是( )
X、Y、Z 三种短周期元素在周期表中的位置如右图,X 通过共用三对电子形成 X2分子,下列说法不正确的是( )| A. | 化合物 XZ3 中各原子均满足 8 电子的稳定结构 | |
| B. | X、Y、Z 三种元素形成的含氧酸都是强酸 | |
| C. | 常温下,Z 单质可与 Y 的氢化物发生置换反应 | |
| D. | 一定条件下,X2与Al反应得到 AlX |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
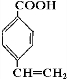
| A. | 该化合物仅含碳、氢两种元素 | B. | 该化合物中碳、氢原子个数比为1:4 | ||
| C. | 无法确定该化合物是否含有氧元素 | D. | 该化合物中一定不含有氧元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
. .
.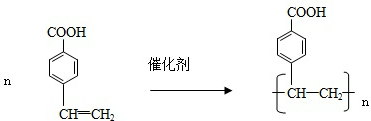 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同时含有分子和离子的电解质溶液,一定是弱电解质溶液 | |
| B. | pH=3的盐酸中,其c(H+)是pH=1的盐酸中的3倍 | |
| C. | 0.1 mol/L KOH溶液和0.1 mol/L 氨水中,其c(OH-)相等 | |
| D. | 室温时,pH=3的硫酸和pH=11的氨水等体积混合,混合溶液的pH>7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 联碱法对母液的处理方法是向母液中通入二氧化碳,冰冻和加食盐 | |
| B. | 列管式热交换器的使用实现了原料的充分利用 | |
| C. | 焙烧辰砂制取汞的反应原理为:HgS+O2$\stackrel{焙烧}{→}$Hg+SO2 | |
| D. | 氯碱工业、铝的冶炼、牺牲阳极的阴极保护法都是应用了电解池的原理 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
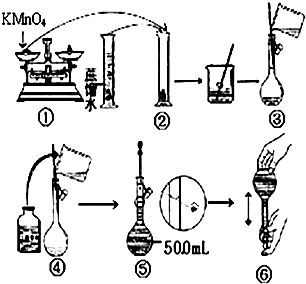 人体血液里Ca2+离子的浓度一般采用g/cm3来表示.抽取一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用KMnO4溶液滴定即可测定血液样品中Ca2+的浓度.某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度:
人体血液里Ca2+离子的浓度一般采用g/cm3来表示.抽取一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用KMnO4溶液滴定即可测定血液样品中Ca2+的浓度.某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入NaOH,溶液pH升高,c(SO32-)增大 | B. | 氯化钡有两性 | ||
| C. | 两支试管中的白色沉淀都是BaSO4 | D. | SO2具有两性且水溶液有酸性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com