

| A、甲装置:可用来除去CO气体中的CO2气体 |
| B、乙装置:可用来验证NaHCO3和Na2CO3的热稳定性 |
| C、丙装置:可用来实验室制备乙酸乙酯 |
| D、丁装置:可用来比较HCl、H2CO3和H2SiO3的酸性强弱 |


科目:高中化学 来源: 题型:
12 6 |
13 6 |
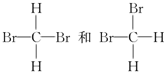 E.CH3CH2CH2CH3和
E.CH3CH2CH2CH3和
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:



查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 下表中各组物质之间不能通过一步反应实现如图的是( )
下表中各组物质之间不能通过一步反应实现如图的是( ) | 甲 | 乙 | 丙 | |
| A | NaHCO3 | Na2CO3 | NaCl |
| B | SiO2 | HSiO3 | Na2SiO3 |
| C | Cl2 | HCl | CuCl2 |
| D | AlCl3 | Al(OH)3 | Al2O3 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、原子半径:W>Z |
| B、最高价氧化物的水化物的酸性:R>W |
| C、气态氢化物的稳定性:X>W |
| D、单质与水(或酸)反应的剧烈程度:Y>Z |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、“类钫”在化合物中是+1价 |
| B、“类钫”具有放射性 |
| C、“类钫”单质的密度大于l g?cm-3 |
| D、“类钫”单质有较高的熔点 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:
元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:| 化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
| 类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
| 熔点/℃ | 2800 | 2050 | 714 | 191 |
| Cl2 |
| 460℃ |
| 蒸馏 |
| H2 |
| 1100℃ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com