
【题目】室温下,在0.2molL﹣1 Al2(SO4)3溶液中,逐滴加入1.0molL﹣1 NaOH溶液,实验测得溶液pH随NaOH溶液体积变化曲线如图,下列有关说法正确的是( ) 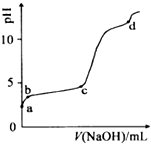
A.a点溶液呈酸性的原因是Al3+水解,离子方程为:Al3++3OH﹣Al(OH)3
B.c点铝元素主要以Al(OH)3的形式存在
C.a﹣b段,溶液pH增大,Al3+浓度不变
D.d点Al(OH)3沉淀开始溶解
【答案】B
【解析】解:室温下,往0.2mol/LAl2 ( SO4)3溶液中逐滴加入1.0mol/L NaOH溶液,硫酸铝为强酸弱碱盐,水解显酸性,水解离子反应为Al3++3H2OAl(OH)3+3H+;a﹣b段,加入NaOH溶液,消耗氢离子,发生反应:H++OH﹣═H2O,b﹣c段溶液的pH变化不大,主要发生反应:Al3++3OH﹣═Al(OH)3↓,则加入的OH﹣主要用于生成Al(OH)3沉淀;c﹣d段溶液pH变化较大,c点后pH发生突变,NaOH过量,Al(OH)3沉淀开始溶解,生成NaAlO2 , 碱性较强,
A.硫酸铝为强酸弱碱盐,铝离子水解导致溶液显酸性,水解离子反应为Al3++3H2OAl(OH)3+3H+ , 故A错误;
B.b﹣c段溶液的pH变化不大,主要发生反应:Al3++3OH﹣═Al(OH)3↓,则加入的OH﹣主要用于生成Al(OH)3沉淀;c﹣d段溶液pH变化较大,c点后pH发生突变,NaOH过量,Al(OH)3沉淀开始溶解,生成NaAlO2 , 所以c点铝元素主要以Al(OH)3的形式存在,故B正确;
C.a﹣b段,发生H++OH﹣═H2O,但加入NaOH溶液,总体积增大,则Al3+浓度减小,故C错误;
D.c点后pH发生突变,NaOH过量,Al(OH)3沉淀开始溶解,生成NaAlO2 , 碱性较强,而d点pH>10,NaOH远远过量,故D错误;
故选B.


科目:高中化学 来源: 题型:
【题目】2016年8月17日,广东警方查获黑窝点非法使用Na2S2O4等浸泡食物来达到保鲜作用,Na2S2O4俗称保险粉,大量用于漂白纸张和印染工业.某学习小组用下列方法制备该物质. ①把甲酸(HCOOH)溶于甲醇溶液,再和足量的NaOH溶液混合配成溶液;
②制取SO2并通入上述溶液中,一段时间后可获得保险粉.
(已知:Na2S2O4在水中溶解度较大,在甲醇中溶解度较小)
装置如图1所示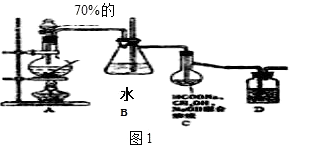
(1)A装置中的分液漏斗改为(仪器名称)更合适,D中盛放的试剂为 .
(2)B装置的作用为;
(3)C装置内发生的化学反应方程式为 .
(4)分离C装置中产品时就选用图2装置中(填甲、乙、丙、丁,下同),回收乙醇的装置为 . 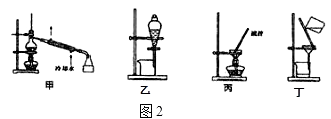
(5)Na2S2O4在碱性环境中除去废水中的CrO42﹣及+4价S的化合物,反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示.下列分析不正确的是( ) 
A.①代表滴加H2SO4溶液的变化曲线
B.b点,溶液中大量存在的离子是Na+、OH﹣
C.c点,两溶液中含有相同量的OH﹣
D.a、d两点对应的溶液均显中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】咖啡酸(如图),存在于许多中药中,如野胡萝卜、光叶水苏、荞麦、木半夏等.咖啡酸有止血作用,特别对内脏的止血效果较好.
(1)咖啡酸的化学式是其中含氧官能团的名称为、 .
(2)咖啡酸可以发生的反应是(填写序号).
①水解反应 ②加成反应 ③酯化反应 ④消去反应
(3)1mol咖啡酸与浓溴水反应时最多消耗mol Br2 .
(4)咖啡酸与NaHCO3溶液反应的方程式
(5)蜂胶的主要活性成分为CPAE,分子式为C17H16O4 , 该物质在一定条件下可水解生成咖啡酸和一种醇,该醇为芳香醇且分子结构中无甲基,此芳香醇的结构简式为 , 咖啡酸跟该芳香醇在一定条件下反应生成CPAE的化学方程式为 . 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列数值关系中不正确的是( )
A. 原子序数=原子核内质子数B. 元素周期表中周期数=原子的电子层数
C. 元素周期表中主族序数=原子的最外层电子数D. 元素的种数=原子种数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某可逆反应为2X(g) ![]() 3Y(g)+Z(g),混合气体中X的物质的量分数与温度关系如图所示:
3Y(g)+Z(g),混合气体中X的物质的量分数与温度关系如图所示:
下列推断正确的是( )。
A.升高温度,该反应平衡常数K减小
B.压强大小有P3>P2>P1
C.平衡后加入高效催化剂使气体相对分子质量增大
D.在该条件下M点X平衡转化率为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用石墨作电极电解CuSO4溶液,通电一段时间后,加入0.3mol的氢氧化铜恰好使电解后溶液复原,则在电解过程中阴极生成H2的物质的量为( )
A.0.15 mol
B.0.3 mol
C.0.45 mol
D.0.6mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1molL﹣1的三种酸(HA、HB和HD)溶液,滴定曲线如图所示,下列判断错误的是( ) 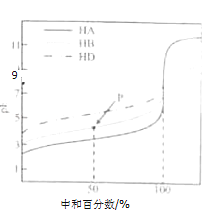
A.三种酸的电离常数关系:KHA>KHB>KHD
B.滴定至P点时,溶液中:c(B﹣)>c(Na+)>c(HB)>c(H+)>c(OH﹣)
C.pH=7时,三种溶液中:c(A﹣)=c(B﹣)=c(D﹣)
D.当中和百分数达100%时,将三种溶液混合后:c(HA)+c(HB)+c(HD)=c(OH﹣)﹣c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com