
| A、Ca2++2OH-=Ca(OH)2↓ CaCO3+2NaOH=Ca(OH)2↓+Na2CO3 |
| B、Ba2++SO42-=BaSO4↓ Ba(OH)2+H2SO4=BaSO4↓+2H2O |
| C、Ag++Cl-=AgCl↓ AgNO3+NaCl=AgCl↓+NaNO3 |
| D、Fe3++3OH-=Fe(OH)3↓ FeCl3+3NH3?H2O=Fe(OH)3↓+3NH4Cl |


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙酸乙酯与氢氧化钠溶液反应:CH3COOC2H5+OH-→CH3COOH+C2H5O- | ||
B、用银氨溶液检验乙醛的醛基:CH3CHO+2Ag(NH3)2++2OH-
| ||
| C、向苯酚钠溶液中通入少量的CO2:CO2+H2O+2C6H5O-→2C6H5OH+2CO32- | ||
| D、甘氨酸与氢氧化钠溶液反应:H2N-CH2COOH+OH-→H2N-CHCOO-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在标准状况下,5.6L四氯化碳含有的分子数为0.25NA |
| B、1mol Cl2参加反应转移的电子数不一定为2NA |
| C、78g Na2O2固体中含有NA个阴离子 |
| D、足量的MnO2与500ml浓盐酸充分反应,产生了NA个Cl2分子,则盐酸的浓度一定大于8 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、无论是风力发电还是潮汐发电,都是将化学能转化为电能 |
| B、光缆在信息产业中有广泛应用,制造光缆的主要材料是单质硅 |
| C、推广燃煤脱硫技术,可以防治SO2污染 |
| D、凡含有食品添加剂的食物对人体健康均有害,不宜食用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ca(OH)2溶液中加入少量NaHCO3溶液:Ca2++2OH-+2HCO3-=CaCO3↓+2H2O+CO32- |
| B、过量氯气通入FeBr2溶液中:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |
| C、二氧化硫气体通入碘水中:SO2+I2+2H2O=2H++SO42-+2HI |
| D、向明矾溶液中加入Ba(OH)2溶液至沉淀质量最大:Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 序号 | 反应 | 平衡常数 |
| 1 | Au+6HNO3(浓)═Au(NO3)3+3NO2↑+3H2O | <<1 |
| 2 | Au3++4Cl-═AuCl4- | K |
查看答案和解析>>
科目:高中化学 来源: 题型:

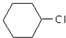 为原料合成重要的化工产品
为原料合成重要的化工产品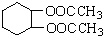 的路线流程图(无机试剂任选)合成路线流程图示例如图2.
的路线流程图(无机试剂任选)合成路线流程图示例如图2.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com