
| A. | HCOOH | B. | HCHO | C. | CH4 | D. | C6H12O6 |
分析 烃及烃的含氧衍生物与在O2中充分燃烧后生成CO2、H2O,通过足量的Na2O2,发生反应2CO2+2Na2O2=2Na2CO3+O2,2H2O+2Na2O2=4NaOH+O2,对生成物变式:Na2CO3~Na2O2•CO,2NaOH~Na2O2•H2,可知过氧化钠增重=与CO2同物质的量的CO质量+与H2O同物质的量的H2质量,组成增重质量的组成可以表示为nCO.mH2,即化学式可以改写成nCO.mH2的物质完全燃烧后过氧化钠增重等于该物质的质量,容器内氧气质量不变,而
反应后容器内氧气质量大于原氧气质量,有机物应为nCO.mH2.xO2形式.
解答 解:烃及烃的含氧衍生物与在O2中充分燃烧后生成CO2、H2O,通过足量的Na2O2,发生反应2CO2+2Na2O2=2Na2CO3+O2,2H2O+2Na2O2=4NaOH+O2,对生成物变式:Na2CO3~Na2O2•CO,2NaOH~Na2O2•H2,可知过氧化钠增重=与CO2同物质的量的CO质量+与H2O同物质的量的H2质量,组成增重质量的组成可以表示为nCO.mH2,即化学式可以改写成nCO.mH2完全燃烧后过氧化钠增重等于该物质的质量,反应后容器内氧气质量大于原氧气质量,有机物应为nCO.mH2.xO2形式,
A.HCOOH可以改写为CO.H2.$\frac{1}{2}$O2形式,故A符合;
B.HCHO可以改写为CO.H2,故B不符合;
C.CH4中没有氧元素,反应后氧气质量小于原氧气质量,故C不符合;
D.C6H12O6以改写为6CO.6H2形式,反应后氧气质量等于原氧气质量,故D不符合,
故选:A.
点评 本题考查化学方程式有关计算,明确反应前后固体质量增加成分是解本题关键,侧重对学生分析能力与方法技巧的考查,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 状态 | 密度/g•cm3 | 沸点/℃熔点/℃ |
| 乙醇 无色液体 | 0.79 | 78.5/-130 |
| 1,2-二溴乙烷 无色液体 | 2.2 | 132/9 |
| 乙醚 无色液体 | 0.71 | 34.6/-116 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 鸡蛋白溶液中分别滴入饱和硫酸铵和醋酸铅溶液 | 均有固体析出 | 均发生变性 |
| B | 溴水中分别加入苯酚和环己烯 | 溴水均褪色 | 均发生加成反应 |
| C | 某无色气体通入溴水中 | 溴水褪色 | 该气体一定是C2H4 |
| D | 适量水玻璃加入稀盐酸中, 振荡得透明溶液,用激光笔照射 | 有丁达尔效应 | 有硅酸胶体生成 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
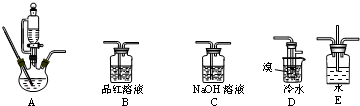
 实验室用如图装置制取少量溴苯,试填写下列空白.
实验室用如图装置制取少量溴苯,试填写下列空白.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl溶液中有杂质Na2SO4(适量的BaCl2溶液) | |
| B. | FeSO4溶液中有杂质CuSO4 (Fe粉) | |
| C. | CO2气体中有少量CO(灼热的氧化铜) | |
| D. | SO2气体中有少量HCl气体(NaOH溶液) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中含有Cl-、C1O-、C1O3-三种含氯元素的离子,其中C1O-、C1O3-两种离子的物质的量(n)与反应时间(t)的曲线如图所示.
在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中含有Cl-、C1O-、C1O3-三种含氯元素的离子,其中C1O-、C1O3-两种离子的物质的量(n)与反应时间(t)的曲线如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com