
使用容量瓶配制溶液时,由于操作不当,会引起误差,下列情况会使所配溶液浓度偏低的是( )
①使用天平(使用游码)称量时,被称量物与砝码位置放颠倒了
②用滴定管量取液体时,开始时平视读数,结束后俯视读数
③溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤
④转移溶液前容量瓶内有少量蒸馏水
⑤定容时,仰视容量瓶刻度线
 ⑥定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
⑥定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
A.①③⑤⑥ B.①②⑤⑥
C.②③④⑥ D.③④⑤⑥
科目:高中化学 来源: 题型:
某含苯环的化合物A,其相对分子质量为104,碳的质量分数为92.3%。
(1)A的分子式为____________。
(2)A与溴的四氯化碳溶液反应的化学方程式为____________,反应类型是____________。

条件下反应的化学方程式________________________。
(4)一定条件下,A与氢气反应,得到的化合物中碳的质量分数为85.7%,写出此化合物的结构简式_______________________。
(5)在一定条件下,由A聚合得到的高分子化合物的结构简式为__________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中,跟100 mL 0.5 mol/L NaCl溶液中所含的Cl-物质的量浓度相同的是( )
A.100 mL 0.5 mol/L MgCl2溶液
B.200 mL 0.25 mol/L AlCl3 溶液
溶液
C.50 mL 1 mol/L NaCl溶液
D.25 mL 0.5 mol/L HCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
V L Fe2(SO4)3溶液中含有a g SO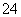 ,取此溶液0.5V L,用水稀释至2V L,则稀释后溶液中Fe3+的物质的量的浓度为( )
,取此溶液0.5V L,用水稀释至2V L,则稀释后溶液中Fe3+的物质的量的浓度为( )
A.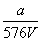 mol/L B.
mol/L B.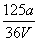 mol/L
mol/L
C. mol/L D.
mol/L D. mol/L
mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
近几年地球发生地震灾害较多,抢救地震后被困在废墟下的伤员,首要的措施是给伤员补充能量。下图是医院给伤员输液时用的一瓶质量分数为5%的葡萄糖(C6H12O6)注射液标签,请认真观察标签上所列的内容后填写:

(1)葡萄糖的摩尔质量为________;
(2)该溶液中 含水________ g;
含水________ g;
(3)该溶液的密度约为________ g/mL;
(4)该溶液的物质的量浓度为________ mol/L(精确到小数点后面两位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
最近科学家冶炼出了纯度高达99.999 9%的铁,据你推测,下列性质它不可能具有的是( )
A、硬度比生铁低
B、在潮湿空气中放置不易生锈
C、在冷的浓硫酸中可钝化
D、与4 mol·L-1盐酸反应的速率比生铁快
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于胶体的说法中正确的是( )
A.溶液和胶体的本质区别是当一束光线通过胶体时可出现一条光亮的通路,溶液则没有此现象
B.制备Fe(OH)3胶体的方法是将饱和氯化铁溶液加热煮沸
C.静电除尘,利用了胶体电泳
D.胶体不均一、不稳定,静置易产生沉淀;溶液均一、稳定,静置不产生沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
溴及其化合物广泛应用于医药、农药、纤维、塑料阻燃剂等,回答下列问题:
(1)海水提溴过程中,向浓缩的海水中通入________,将其中的Br-氧化,再用空气吹出溴;然后用碳酸钠溶液吸收溴,溴歧化为Br-和BrO ,其离子方程式为__________________________________________。
,其离子方程式为__________________________________________。
(2)溴与氯能以共价键结合形成BrCl。BrCl分子中,________显正电性。BrCl与水发生反应的化学方程式为____________________________________________。
(3)CuBr2分解的热化学方程式为:
2CuBr2(s)===2CuBr(s)+ Br2(g)
ΔH=+105.4 kJ/mol
在密闭容器中将过量CuBr2于487 K下加热分解,平衡时p(Br2)为4.66×103 Pa。
①如反应体系的体积不变,提高反应温度,则p(Br2)将会________(填“增大”“不变”或“减小”)。
②如反应温度不变,将反应体系的体积增加一倍,则p(Br2)的变化范围为__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com