
 £®Čē¹ūA”¢B¾łÓÉČżÖÖŌŖĖŲ×é³É£¬BĪŖĮ½ŠŌ²»ČÜĪļ£¬ŌņÓÉAÓė¹żĮæµÄC·“Ó¦×Ŗ»ÆĪŖBµÄĄė×Ó·½³ĢŹ½ĪŖAlO2-+CO2+2H2O=Al£ØOH£©3”ż+HCO3-£®
£®Čē¹ūA”¢B¾łÓÉČżÖÖŌŖĖŲ×é³É£¬BĪŖĮ½ŠŌ²»ČÜĪļ£¬ŌņÓÉAÓė¹żĮæµÄC·“Ó¦×Ŗ»ÆĪŖBµÄĄė×Ó·½³ĢŹ½ĪŖAlO2-+CO2+2H2O=Al£ØOH£©3”ż+HCO3-£®·ÖĪö £Ø1£©X”¢Y”¢Z”¢Q”¢RŹĒĪåÖÖ¶ĢÖÜĘŚŌŖĖŲ£¬Ō×ÓŠņŹżŅĄ“ĪŌö“ó£®XŹĒŌ×Ó°ė¾¶×īŠ”µÄÖ÷×åŌŖĖŲ£¬ŌņXĪŖHŌŖĖŲ£»Z”¢R·Ö±šŹĒµŲæĒÖŠŗ¬Įæ×īøߵķĒ½šŹōŌŖĖŲŗĶ½šŹōŌŖĖŲ£¬ŌņZĪŖOŌŖĖŲ”¢RĪŖAl£»YŌŖĖŲ×īøßÕż¼ŪÓė×īµĶøŗ¼ŪÖ®ŗĶĪŖ0£¬ÓÉŌ×ÓŠņŹżæÉÖŖ£¬Ö»ÄÜ“¦ÓŚµŚ¢ōA×壬¶ųĘäŌ×ÓŠņŹżÓÖŠ”ÓŚOŌŖĖŲ£¬¹ŹYĪŖĢ¼ŌŖĖŲ£»QÓėXĶ¬Ö÷×壬½įŗĻŌ×ÓŠņŹżæÉÖŖQĪŖNa£»
£Ø2£©¢Ł¼ĘĖćÉś³É2mol°±Ęų·Å³öµÄČČĮ棬עĆ÷ĪļÖŹµÄ¾Ū¼ÆדĢ¬Óė·“Ó¦Čȏ銓ČČ»Æѧ·½³ĢŹ½£»
¢Ś·“Ó¦ČČ=·“Ó¦Īļ×ܼüÄÜ-Éś³ÉĪļ×ܼüÄÜ£»
£Ø3£©Ōµē³Ųøŗ¼«·¢ÉśŃõ»Æ·“Ó¦£¬°±ĘųŌŚøŗ¼«Ź§Č„µē×Ó£¬¼īŠŌĢõ¼žĻĀÉś³ÉµŖĘųÓėĖ®£®
½ā“š ½ā£ŗ£Ø1£©X”¢Y”¢Z”¢Q”¢RŹĒĪåÖÖ¶ĢÖÜĘŚŌŖĖŲ£¬Ō×ÓŠņŹżŅĄ“ĪŌö“ó£®XŹĒŌ×Ó°ė¾¶×īŠ”µÄÖ÷×åŌŖĖŲ£¬ŌņXĪŖHŌŖĖŲ£»Z”¢R·Ö±šŹĒµŲæĒÖŠŗ¬Įæ×īøߵķĒ½šŹōŌŖĖŲŗĶ½šŹōŌŖĖŲ£¬ŌņZĪŖOŌŖĖŲ”¢RĪŖAl£»YŌŖĖŲ×īøßÕż¼ŪÓė×īµĶøŗ¼ŪÖ®ŗĶĪŖ0£¬ÓÉŌ×ÓŠņŹżæÉÖŖ£¬Ö»ÄÜ“¦ÓŚµŚ¢ōA×壬¶ųĘäŌ×ÓŠņŹżÓÖŠ”ÓŚOŌŖĖŲ£¬¹ŹYĪŖĢ¼ŌŖĖŲ£»QÓėXĶ¬Ö÷×壬½įŗĻŌ×ÓŠņŹżæÉÖŖQĪŖNa£»
¢ŁĖłÓŠŌŖĖŲÖŠHŌ×Ó°ė¾¶×īŠ”£¬Ķ¬ÖÜĘŚ×Ō×ó¶ųÓŅŌ×Ó°ė¾¶¼õŠ””¢·Ē½šŹōŌöĒ棬Ķ¬Ö÷×å×ŌÉĻ¶ųĻĀŌ×Ó°ė¾¶Ōö“󔢷Ē½šŹōŠŌ¼õČõ£¬¹ŹÉĻŹöĪåÖÖŌŖĖŲÖŠ£¬NaµÄŌ×Ó°ė¾¶×ī“ó£¬OµÄ·Ē½šŹōŠŌ×īĒ棬
¹Ź“š°øĪŖ£ŗNa£»O£»
¢ŚHÓėCÄÜŠĪ³É¶ąÖÖ»ÆŗĻĪļ£¬ĘäÖŠ¼Čŗ¬¼«ŠŌ¼üÓÖŗ¬·Ē¼«ŠŌ¼ü£¬ĒŅĻą¶Ō·Ö×ÓÖŹĮæ×īŠ”µÄĪļÖŹĪŖC2H2£¬
¹Ź“š°øĪŖ£ŗC2H2£»
¢ŪÓÉŅŌÉĻijŠ©ŌŖĖŲ×é³ÉµÄ»ÆŗĻĪļA”¢B”¢C”¢DÓŠČēĻĀ×Ŗ»Æ¹ŲĻµ£ŗA$?_{D}^{C}$B£ØŌŚĖ®ČÜŅŗÖŠ½ųŠŠ£©£¬ĘäÖŠCŹĒČÜÓŚĖ®ĻŌĖįŠŌµÄĘųĢ壬ŌņCĪŖCO2£¬DŹĒµ»ĘÉ«¹ĢĢåŌņDĪŖNa2O2£¬Na2O2µÄµē×ÓŹ½ĪŖ £»
£»
Čē¹ūA”¢B¾łÓÉČżÖÖŌŖĖŲ×é³É£¬BĪŖĮ½ŠŌ»ÆŗĻĪļ£¬ĒŅ²»ČÜÓŚĖ®£¬ŌņBĪŖAl£ØOH£©3£¬AĪŖNaAlO2£¬¼×Óė¹żĮæµÄCO2·“Ӧɜ³ÉÉś³ÉĒāŃõ»ÆĀĮ³ĮµķÓėĢ¼ĖįĒāÄĘ£¬·“Ó¦Ąė×Ó·½³ĢŹ½ĪŖ£ŗAlO2-+CO2+2H2O=Al£ØOH£©3”ż+HCO3-£¬
¹Ź“š°øĪŖ£ŗ £»AlO2-+CO2+2H2O=Al£ØOH£©3”ż+HCO3-£»
£»AlO2-+CO2+2H2O=Al£ØOH£©3”ż+HCO3-£»
£Ø2£©¢ŁÉś³É2mol°±Ęų·Å³öµÄČČĮæĪŖ46.1kJ”Į2=92.2kJ£¬·“Ó¦ČČ»Æѧ·½³ĢŹ½ĪŖ£ŗN2£Øg£©+3H2£Øg£©?2NH3£Øg£©”÷H=-92.2kJ/mol£¬
¹Ź“š°øĪŖ£ŗN2£Øg£©+3H2£Øg£©?2NH3£Øg£©”÷H=-92.2kJ/mol£»
¢ŚÉč¶ĻæŖ1mol N-H¼üĖłŠčµÄÄÜĮæŹĒxkJ£¬Ōņ945.8kJ/mol+3”Į436.0kJ/mol-6”ĮxkJ/mol=-92.2kJ/mol£¬½āµĆx=391£¬
¹Ź“š°øĪŖ£ŗ391£»
£Ø3£©Ōµē³Ųøŗ¼«·¢ÉśŃõ»Æ·“Ó¦£¬°±ĘųŌŚøŗ¼«Ź§Č„µē×Ó£¬¼īŠŌĢõ¼žĻĀÉś³ÉµŖĘųÓėĖ®£¬øŗ¼«µē¼«·“Ó¦Ź½ĪŖ£ŗ2NH3+6OH--6e-=N2+6H2O£¬
¹Ź“š°øĪŖ£ŗ2NH3+6OH--6e-=N2+6H2O£®
µćĘĄ ±¾Ģāæ¼²é½į¹¹ŠŌÖŹĪ»ÖĆ¹ŲĻµÓ¦ÓĆ”¢ČČ»Æѧ·½³ĢŹ½ŹéŠ“”¢¼üÄÜÓė·“Ó¦ČČ¹ŲĻµ”¢Ōµē³ŲµČ£¬ĶʶĻŌŖĖŲŹĒ½āĢāµÄ¹Ų¼ü£¬×¢ŅāŌŖĖŲ×īøßÕż¼ŪÓė×īµĶøŗ¼ŪÖ®ŗĶ¾łĪŖ0£¬æÉŅŌĪŖ¢ōA×åŌŖĖŲ£¬Ņ²æÉŅŌĪŖHŌŖĖŲ£¬ÖŠŃ§ÖŠ½ĻÉŁÉę¼°HŌŖĖŲµÄøŗ»ÆŗĻ¼Ū£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| Ö÷×å ÖÜĘŚ | ¢ńA | ¢ņA | ¢óA | ¢ōA | ¢õA | ¢öA | ¢÷A | 0 |
| 2 | C | N | O | |||||
| 3 | Na | Mg | Si | S | Cl | Ar | ||
| 4 | Ca |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £®
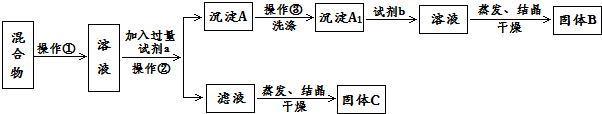
£® £®Ķ¬Ź±Āś×ćĻĀĮŠĢõ¼žµÄBµÄĶ¬·ÖŅģ¹¹Ģå£Ø²»°üĄØB£©¹²ÓŠ11ÖÖ£ŗÄÜÓėFeCl3ČÜŅŗĻŌ×ĻÉ«£¬±½»·ÉĻÖ»ÓŠĮ½øöČ”“ś»ł£®
£®Ķ¬Ź±Āś×ćĻĀĮŠĢõ¼žµÄBµÄĶ¬·ÖŅģ¹¹Ģå£Ø²»°üĄØB£©¹²ÓŠ11ÖÖ£ŗÄÜÓėFeCl3ČÜŅŗĻŌ×ĻÉ«£¬±½»·ÉĻÖ»ÓŠĮ½øöČ”“ś»ł£® £ØČĪŠ“Ņ»ÖÖ£©£®
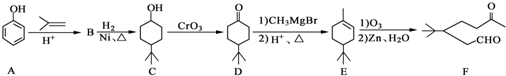
£ØČĪŠ“Ņ»ÖÖ£©£®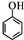 £©ŗĶCH2=CH2ĪŖŌĮĻÖʱøÓŠ»śĪļ
£©ŗĶCH2=CH2ĪŖŌĮĻÖʱøÓŠ»śĪļ  µÄŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼£ØĪŽ»śŹŌ¼ĮČĪÓĆ£©£®ŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼Ź¾ĄżČēĻĀ£ŗ
µÄŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼£ØĪŽ»śŹŌ¼ĮČĪÓĆ£©£®ŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼Ź¾ĄżČēĻĀ£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 35g | B£® | 30g | C£® | 20g | D£® | 15g |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
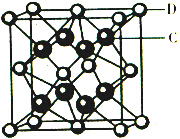 ŅŃÖŖA”¢B”¢C”¢D”¢E¶¼ŹĒŌŖĖŲÖÜĘŚ±ķÖŠĒ°36ŗŵÄŌŖĖŲ£¬ĖüĆĒµÄŌ×ÓŠņŹżŅĄ“ĪŌö“ó£®AŌ×Ó»łĢ¬Ź±×īĶā²ćµē×ÓŹżŹĒĘäÄŚ²ćµē×Ó×ÜŹżµÄ2±¶£¬BŌ×Ó»łĢ¬Ź±sµē×ÓŹżÓėPµē×ÓŹżĻąµČ£¬CŌŚŌŖĖŲÖÜĘŚ±ķµÄø÷ŌŖĖŲÖŠµēøŗŠŌ×ī“ó£¬DµÄ»łĢ¬Ō×ÓŗĖĶāÓŠ6øöÄܼ¶ĒŅČ«²æ³äĀśµē×Ó£¬EŌ×Ó»łĢ¬Ź±Ī“³É¶Ōµē×ÓŹżŹĒĶ¬ÖÜĘŚŌŖĖŲÖŠ×ī¶ąµÄ£®FŌ×ÓŗĖĶā×īĶā²ćµē×ÓŹżÓėNaĻąĶ¬£¬ĘäÓąø÷²ćµē×Ó¾ł³äĀś£®
ŅŃÖŖA”¢B”¢C”¢D”¢E¶¼ŹĒŌŖĖŲÖÜĘŚ±ķÖŠĒ°36ŗŵÄŌŖĖŲ£¬ĖüĆĒµÄŌ×ÓŠņŹżŅĄ“ĪŌö“ó£®AŌ×Ó»łĢ¬Ź±×īĶā²ćµē×ÓŹżŹĒĘäÄŚ²ćµē×Ó×ÜŹżµÄ2±¶£¬BŌ×Ó»łĢ¬Ź±sµē×ÓŹżÓėPµē×ÓŹżĻąµČ£¬CŌŚŌŖĖŲÖÜĘŚ±ķµÄø÷ŌŖĖŲÖŠµēøŗŠŌ×ī“ó£¬DµÄ»łĢ¬Ō×ÓŗĖĶāÓŠ6øöÄܼ¶ĒŅČ«²æ³äĀśµē×Ó£¬EŌ×Ó»łĢ¬Ź±Ī“³É¶Ōµē×ÓŹżŹĒĶ¬ÖÜĘŚŌŖĖŲÖŠ×ī¶ąµÄ£®FŌ×ÓŗĖĶā×īĶā²ćµē×ÓŹżÓėNaĻąĶ¬£¬ĘäÓąø÷²ćµē×Ó¾ł³äĀś£®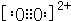 £¬1mol B22+ÖŠŗ¬ÓŠµÄ¦Š¼üŹżÄæĪŖ2NA£®
£¬1mol B22+ÖŠŗ¬ÓŠµÄ¦Š¼üŹżÄæĪŖ2NA£® øĆĄė×Ó»ÆŗĻĪļ¾§ĢåµÄĆܶČĪŖa g/cm3£¬Ōņ¾§°ūµÄĢå»żŹĒ$\frac{312}{a{N}_{A}}$ cm3£ØÖ»ŅŖĒóĮŠĖćŹ½£¬°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµĪŖNA£©£®
øĆĄė×Ó»ÆŗĻĪļ¾§ĢåµÄĆܶČĪŖa g/cm3£¬Ōņ¾§°ūµÄĢå»żŹĒ$\frac{312}{a{N}_{A}}$ cm3£ØÖ»ŅŖĒóĮŠĖćŹ½£¬°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµĪŖNA£©£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

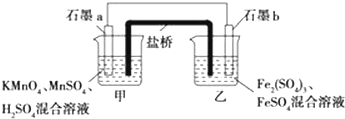
| A£® | Ōµē³ŲµÄ×Ü·“Ó¦ĪŖFe+Cu2+ØTFe2++Cu | |
| B£® | ŃĪĒÅÖŠŹĒKNO3ČÜŅŗ£¬ŌņŃĪĒÅÖŠNO3-ŅĘĻņŅŅÉÕ± | |
| C£® | ĘäĖūĢõ¼ž²»±ä£¬Čō½«CuCl2ČÜŅŗ»»ĪŖNH4ClČÜŅŗ£¬ŹÆÄ«µē¼«·“Ó¦Ź½ĪŖ2H++2e-ØTH2”ü | |
| D£® | ·“Ó¦Ē°£¬µē¼«ÖŹĮæĻąµČ£¬Ņ»¶ĪŹ±¼äŗó£¬Į½µē¼«ÖŹĮæĻą²ī12g£¬µ¼ĻßÖŠĶعż0.2molµē×Ó |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com