
(6分)某些非金属元素的单质和化合物在一定条件下有如下图的转化关系,其中A为单质,D为最高价氧化物对应的水化物。

若A为淡黄色固体,反应②的化学方程式:________________________
若C为红棕色气体,则A的电子式为_______________________________
反应①中的氧化剂是__________还原剂是_______________________
反应②的离子方程式:_______________________________________________
科目:高中化学 来源:2013届四川省高二上学期期中考试化学试卷 题型:填空题
(11分)下表为长式周期表的一部分,其中的编号代表对应的元素。
|
① |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
② |
|
|
|
|
|
|
|
|
|
|
|
③ |
|
|
|
|
|
|
④ |
|
|
|
|
|
|
|
|
|
|
⑤ |
|
⑥ |
|
⑦ |
|
|
|
⑧ |
|
|
|
|
|
|
|
|
⑨ |
|
|
|
|
|
|
|
请回答下列问题:
(1)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为 ;③和⑦形成的一种常见溶剂的化学式为 ,其立体构型为________________。
(2)某元素原子的外围电子排布式为nsnnpn+1,该元素原子的最外电子层上孤电子对数为 ;该元素与元素①形成的最简单分子X属于 分子(填“极性”或“非极性”)。
(3)元素④的第一电离能 元素⑤(选填“>”、“=”、“<”)的第一电离能;元素⑥的电负性 元素⑦(选填“>”、“=”、“<”)的电负性。
(4)元素⑦和⑧形成的化合物的电子式为 。
(5)元素⑨的基态原子核外电子排布式是 。
(6)某些不同族元素的性质也有一定的相似性,如上表中元素②与元素⑤的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:
__________________________________________________________________________
查看答案和解析>>
科目:高中化学 来源:模拟题 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:
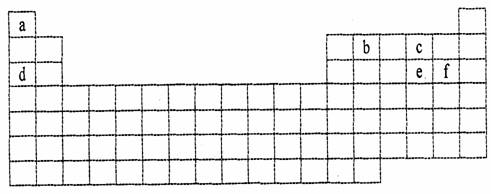
(10分)下图是元素周期表的框架,标有a、b、c、d、e、f 六种元素的位置。
![]()
![]() 据此回答下列问题:
据此回答下列问题:
(1)请用实线画出上面的元素周期表中金属元素与非金属元素的分界线。
(2) a、b、c、d 四种元素的原子半径由大到小的顺序依次是___________________。
(3)由a、c、f 三种元素形成的强酸的化学式是______________________。
(4)在上述六种元素中,金属性最强的是(填元素符号)_________;过渡元素位于元素周期表中第____________~___________纵行。
( 5 ) b 与c 形成的化合物的电子式为_____________________________。
( 6 )A.主族元素都是非金属元素 B.主族元素都是金属元素
C.非金属元素都位于短周期 D.非金属元素都不在副族
(7)由a、c形成的一种化合物与c、e 形成的一种化合物发生氧化还原反应,生成一种强酸,请写出该反应的化学方程式____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)氯气能从碘化钾中将碘置换出来。据此判断氯元素和碘元素非金属性的强弱。
(2)磷元素和硫元素的最高正化合价分别为+5、+6,且磷元素的非金属性弱于硫元素。请写出这两种元素最高价氧化物对应水化物的化学式,并比较它们酸性的强弱。
(3)H2SO4、H2SeO4分别是硫元素和硒元素最高正价氧化物对应的水化物,且H2SO4的酸性强于H2SeO4。据此判断硫元素和硒元素氧化能力的强弱。
(4)溴单质在加热的条件下可与氢气化合生成HBr,碘单质在高温条件下才能与氢气化合生成HI。据此判断HBr和HI稳定性的强弱。
(5)请用一个化学反应事实说明氟的非金属性强于氧,并写出相关的化学反应方程式。
(6)说明氯元素的非金属性强于溴元素的化学事实有哪些?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com