
| A. | 乙酸乙酯和水,乙醇和水,己烯和水 | |
| B. | 二溴乙烷和水,溴苯和水,硝基苯和水 | |
| C. | 己烷和水,乙醛和水,乙酸和乙醇 | |
| D. | 乙酸和水,甲苯和水,己烷和己烯 |
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 空气质量日报列入的首要主要污染物有二氧化硫、二氧化氮和可吸入颗粒物等 | |
| B. | 酸雨是指pH小于7的雨水 | |
| C. | 为了减少二氧化硫和二氧化氮的排放,工业废气排放到大气之前必须进行回收处理 | |
| D. | 含磷合成洗涤剂直接排放会导致水体污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 电池工作时,负极附近溶液的pH升高 | |
| B. | 电路中转移2mol电子,理论上约消耗标准状况下空气56L | |
| C. | 电池工作时,电流由M极经外电路流向N极 | |
| D. | 电池总反应为4Al+3O2=2Al2O3、2Mg+O2=2MgO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 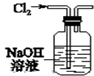 用图装置除去Cl2中混有的少量HCl | |
| B. | 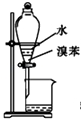 用图装置分离水和溴苯的混合物 | |
| C. | 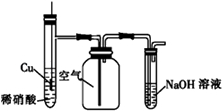 用图装置制备并收集NO气体 | |
| D. | 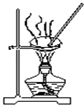 用图装置蒸干AlCl3饱和溶液制备AlCl3晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 写成2aA+2bB?2cC,Q值、K值均扩大了一倍 | |
| B. | 写成2aA+2bB?2cC,Q值扩大了一倍,K值保持不变 | |
| C. | 写成cC?aA+bB,Q值、K值变为原来的相反数 | |
| D. | 写成cC?aA+bB,Q值变为原来的相反数,K值变为倒数 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乳酸薄荷醇酯( 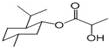 )仅能发生水解、氧化、消去反应 )仅能发生水解、氧化、消去反应 | |
| B. | 乙醛和丙烯醛( )不是同系物,它们与氢气充分反应后的产物也不是同系物 )不是同系物,它们与氢气充分反应后的产物也不是同系物 | |
| C. | 油脂在碱性条件下水解生成高级脂肪酸和甘油 | |
| D. | CH3COOCH2CH3 与CH3CH2COOCH3 互为同分异构体,1H-NMR谱显示两者均有三种不同的氢原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
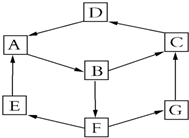 某兴趣活动小组利用物质间的互变,设计成一个平面魔方,如图所示:
某兴趣活动小组利用物质间的互变,设计成一个平面魔方,如图所示:| 纯A(单质) | B溶液 | D固体 | G溶液 | |
| 颜色 | 银白色 | 黄色 | 红棕色 | 浅绿色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com