
| A.完全溶解89g针铁矿,需要1.5mol/L的稀盐酸至少2L |
| B.针铁矿的化学式是FeO(OH) |
| C.针铁矿中铁元素为+3价 |
| D.44.5g针铁矿约含有6.02×1023个O2。 |
科目:高中化学 来源:不详 题型:实验题
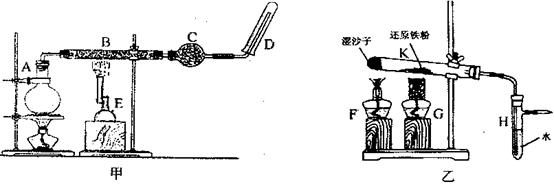
 装置的尖嘴导管处点燃反应产生的气体,装置H必不可少,H的作用是 。
装置的尖嘴导管处点燃反应产生的气体,装置H必不可少,H的作用是 。
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
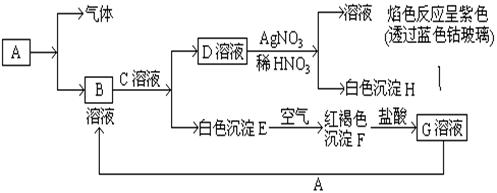
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
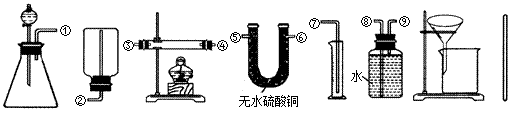
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Mg、Fe混合物总物质的量为0.5 mol |
| B.Mg与Fe物质的量之比为3︰1 |
| C.生成MgSO4的质量为45 g |
| D.该稀硫酸物质的量浓度为0.5 mol/L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.若反应后有Cu剩余,则反应后溶液中含有的金属阳离子一定是Cu2+ |
| B.若反应后的溶液中有Cu2+,则反应后溶液中含有的金属阳离子一定是Fe2+、Fe3+ |
| C.若反应后的溶液中无金属剩余,则加入金属粉末质量8.4 g<a<9.6 g |
| D.若加入的Fe和Cu的质量比为7:8,则使HN03完全反应的金属粉末质量最小为7.2 g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.可表示为3YO3·3FeO·Fe2O3 | B.可表示为Y3O5·Fe3O4·Fe2O3 |
| C.其中钇、铁的化合价均为+3价 | D.其中钇、铁的化合价均有+2、+3价 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com