
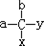 中,当a、b、x、y为彼此互不相同的原子或原子团时,称此分子为手性分子,中心碳原子为手性碳原子.下列分子中指定的碳原子(用*标记)不属于手性碳原子的是( )
中,当a、b、x、y为彼此互不相同的原子或原子团时,称此分子为手性分子,中心碳原子为手性碳原子.下列分子中指定的碳原子(用*标记)不属于手性碳原子的是( )| A. | 苹果酸: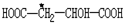 | B. | 丙氨酸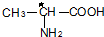 | C. | 葡萄糖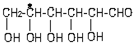 | D. | 甘油醛 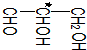 |
分析 手性碳原子指连有四个不同基团的碳原子,手性碳原子判断注意:1、手性碳原子一定是饱和碳原子;2、手性碳原子所连接的四个基团要是不同的.
解答 解:A、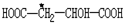 中*号碳原子上连有两个一样的氢原子,不是手性碳原子,故A正确;
中*号碳原子上连有两个一样的氢原子,不是手性碳原子,故A正确;
B、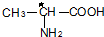 中*号碳原子上连有四个不一样的基团:氢原子、甲基、羧基和氨基,是手性碳原子,故B错误;
中*号碳原子上连有四个不一样的基团:氢原子、甲基、羧基和氨基,是手性碳原子,故B错误;
C、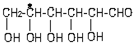 中*号碳原子上连有四个不一样的基团:氢原子、-CH2OH、羟基以及剩余的大取代基,是手性碳原子,故C错误;
中*号碳原子上连有四个不一样的基团:氢原子、-CH2OH、羟基以及剩余的大取代基,是手性碳原子,故C错误;
D、 中*号碳原子上连有四个不一样的基团:氢原子、-CH2OH、羟基以及醛基,是手性碳原子,故D错误.
中*号碳原子上连有四个不一样的基团:氢原子、-CH2OH、羟基以及醛基,是手性碳原子,故D错误.
故选A.
点评 本题主要考查学生手性碳原子的确定方法,注意手性碳原子一定是饱和碳原子且手性碳原子所连接的四个基团要是不同的,难度不大.


 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源: 题型:选择题
| A. | 铜和硝酸反应 | B. | 锌和氯化铁溶液反应 | ||
| C. | 细铁丝在氯气中燃烧 | D. | 氯化铝与氢氧化钠溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素的原子半径:A<B<C<D<E | |
| B. | 对应氢化物的热稳定性:D>E | |
| C. | B与C、B与D形成的化合物中化学键类型相同 | |
| D. | 五种元素中最高价氧化物对应的水化物酸性最强的是E |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
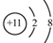 .
.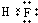 、
、 ,属于两性化合物的电离方程式Al3++3OH-?Al(OH)3 ?H++AlO2-+H2O.
,属于两性化合物的电离方程式Al3++3OH-?Al(OH)3 ?H++AlO2-+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知:2X(g)+Y(g)?a Z(g),在T1温度下,体积为2L的密闭容器中,充入6mol X和2mol Y.根据图示回答:
已知:2X(g)+Y(g)?a Z(g),在T1温度下,体积为2L的密闭容器中,充入6mol X和2mol Y.根据图示回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯原子的结构示意图: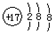 | |
| B. | 乙烯的结构简式为CH2CH2 | |
| C. | 氯化镁的电子式: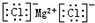 | |
| D. | 硫酸的电离方程式:H2SO4═H2++SO42ˉ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜的金属活泼性比铁的弱,可在海轮外壳上装若干铜块以减缓其腐蚀 | |
| B. | 液氨汽化时要吸收大量的热,可用作制冷剂 | |
| C. | 生石灰能与水反应,可用来干燥氯气 | |
| D. | 二氧化硅不与强酸反应,可用石英作为反应容器制取氢氟酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | K2CO3 | KHCO3 | K2SO4 | KMnO4 |
| 溶解度g/100g | 111 | 33.7 | 11.1 | 6.34 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com