
| A. | 气体乙和气体丙都为纯净物 | |
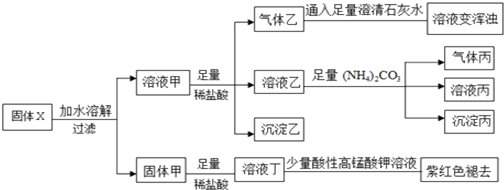
| B. | 固体粉末X中一定含有FeO、Na2S2O3、NaAlO2、Na2CO3,可能含有NaHCO3 | |
| C. | 溶液丁中的阳离子可能只含H+、Fe2+ | |
| D. | 溶液甲中一定含有AlO2-、CO32-、HCO3- |
分析 根据X是否溶于水,分为两部分;固体甲溶于足量盐酸,能使酸性高锰酸钾褪色,可知含有溶液丁中的阳离子一定含H+、Fe2+,可能含有Fe3+,X一定含有FeO;溶液甲加入足量稀盐酸,产生气体和沉淀,说明X一定含有Na2S2O3、NaAlO2,加入碳酸氢铵生成沉淀,说明AlO2-一定存在,而HCO3- 与AlO2-不共存,一定不含NaHCO3,可能含有Na2CO3,以此解答该题.
解答 解:根据X是否溶于水,分为两部分;固体甲溶于足量盐酸,能使酸性高锰酸钾褪色,可知含有溶液丁中的阳离子一定含H+、Fe2+,可能含有Fe3+,X一定含有FeO;溶液甲加入足量稀盐酸,产生气体和沉淀,说明X一定含有Na2S2O3、NaAlO2,加入碳酸氢铵生成沉淀,说明AlO2-一定存在,而HCO3- 与AlO2-不共存,一定不含NaHCO3,可能含有Na2CO3;
A.由以上分析可知,乙可能是二氧化碳和二氧化硫,故A错误;
B.粉末X 中一定含有FeO、Na2S2O3、NaAlO2,一定不含NaHCO3,因为HCO3- 与AlO2-不共存,故B错误;
C.溶液丁中的阳离子一定含H+、Fe2+,可能含有Fe3+,故C正确;
D.溶液甲中一定含有AlO2-,可能含有CO32-,故D错误;
故选C.
点评 本题考查物质的检验和鉴别的实验方案的设计,侧重于元素化合物知识的综合运用,题目难度中等,注意把握反应的现象,根据现象结合物质的性质进行判断.


 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
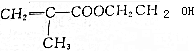 ,下列说法错误的是( )
,下列说法错误的是( )| A. | M能发生加成反应 | |
| B. | M能发生取代反应 | |
| C. | 一定条件下,M能与乙醇发生酯化反应 | |
| D. | M既能使溴水褪色,也能使酸性高锰酸钾溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol•L-1FeCl3溶液中:K+、Na+、AlO2-、SCN- | |
| B. | 能溶解CaCO3的溶液中:Fe2+、Ca2+、Cl-、NO${\;}_{{3}_{\;}^{\;}}^{-}$ | |
| C. | 澄清透明的溶液中:Cu2+、Mg2+、SO${\;}_{4}^{2-}$、Cl- | |
| D. | 由水电离得到的c(H+)=1×10-13mol•L-1的溶液中:Mg2+、Cu2+、SO42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
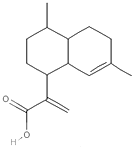
| A. | 能发生酯化反应 | B. | 属于芳香族化合物 | ||
| C. | 能与NaHCO3溶液反应 | D. | 能使溴的四氯化碳溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com