
| A. | 根据是否含有氧元素,将物质分为氧化剂和还原剂 | |
| B. | 根据是否具有丁达尔现象,将分散系分为溶液、胶体和浊液 | |
| C. | 根据水溶液是否能够导电,将物质分为电解质和非电解质 | |
| D. | 根据反应中是否有电子转移,将化学反应分为氧化还原反应和非氧化还原反应 |
分析 A.反应物中含元素化合价升高的物质为还原剂,含元素化合价降低的物质为氧化剂;
B.分散系的分类依据是根据分散系微粒直径的大小;
C.电解质是指在水溶液里或熔化状态下能够导电的化合物,非电解质是指在水溶液里和熔化状态下都不能够导电的化合物;
D.氧化还原反应中有电子的转移,而非氧化还原反应物电子的转移.
解答 解:A.根据反应物中含元素化合价升降,将物质分为氧化剂和还原剂,故A错误;
B.分散系的分类依据是根据分散系中分散质粒子直径的大小,而不是否具有丁达尔现象,故B错误;
C.根据在水溶液里或熔化状态下能否导电,将物质分为电解质和非电解质,故C错误;
D.根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应,故D正确.
故选D.
点评 本题考查物质的分类,题目难度不大,注意物质的分类的依据,试题培养了学生灵活应用所学知识的能力.


科目:高中化学 来源: 题型:选择题
| A. |  | B. |  | C. |  | D. |  |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(A)═0.01 mol/(L•s) | B. | v (B)═0.02 mol/(L•s) | ||
| C. | v (B)═0.60mol/(L•min) | D. | v (C)═1.0mol/(L•min) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 邻甲基苯酚能与NaOH溶液反应而苯甲醇不能 | |
| B. | 等物质的量的乙醇和乙二醇与足量的金属钠反应,后者产生的氢气比前者多 | |
| C. | 苯与液溴在催化剂存在下发生反应,而苯酚与浓溴水混合就能发生反应 | |
| D. | 甲苯能使酸性高锰酸钾溶液褪色而甲烷不能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体的分散质粒子能通过滤纸,而其他分散系的分散质粒子不能通过滤纸 | |
| B. | 氢氧化铁胶体、硫酸铜溶液用激光笔照射,均能观察到一条光亮的通道 | |
| C. | 胶体区分于溶液的本质特征是胶体的分散质粒子直径在1nm~100nm之间 | |
| D. | 氢氧化铝和氢氧化铁胶体可用于净水是因为它们具有强氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
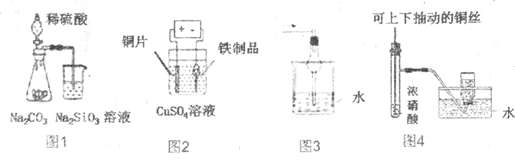
| A. | 图1为证明非金属性强弱:S>C>Si | |
| B. | 图2为在铁制品表面镀铜 | |
| C. | 图3可用于吸收氯化氢、溴化氢等气体 | |
| D. | 图4为制备并收集少量NO2气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 2.4g金属镁所含电子数目为0.2NA | B. | 16gCH4所含原子数目为NA | ||
| C. | 17gNH3所含电子数目为10NA | D. | 18g水所含分子数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某校化学兴趣小组探究SO2与FeCl3溶液的反应,所用装置如图所示.
某校化学兴趣小组探究SO2与FeCl3溶液的反应,所用装置如图所示.| 步骤① | 配制1mol•L-1 FeCl3溶液(未用盐酸酸化),测其pH约为1,取少量装入试管B中,加热A. |
| 步骤② | 往5mL 1mol•L-1 FeCl3溶液中通入SO2气体,溶液立即变为红棕色.微热3min,溶液颜色变为浅绿色. |
| 步骤③ | 往5mL重新配制的1mol•L-1 FeCl3溶液(用浓盐酸酸化)中通入SO2气体,溶液立即变为红棕色.几分钟后,发现溶液颜色变成浅绿色. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 以Mg2+为中心的大环配合物叶绿素能催化光合作用 | |
| B. | Fe2+的卟啉配合物是输送O2的血红素 | |
| C. | 三价铁离子和硫氰酸根离子形成的配离子常用于人造血液 | |
| D. | 钴离子的卟啉配合物是人体需要的一种维生素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com