


 金钥匙试卷系列答案
金钥匙试卷系列答案科目:高中化学 来源: 题型:
| O2 |
| ① |
| O2 |
| ② |
| H2O |
| ③ |
| Cu |
| ④ |
| BaCl2 |
| ⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
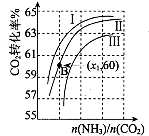 用氨合成尿素的反应为2NH3(g)+CO2(g)?CO(NH2)2(1)+H2O(g).工业生产时,原料气带有水蒸气.图表示CO2的转化率与氨碳比
用氨合成尿素的反应为2NH3(g)+CO2(g)?CO(NH2)2(1)+H2O(g).工业生产时,原料气带有水蒸气.图表示CO2的转化率与氨碳比| n(NH3) |
| n(CO2) |
| n(H2O) |
| n(CO2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,离子反应方程式为
(1)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,离子反应方程式为查看答案和解析>>
科目:高中化学 来源: 题型:
| A、10 mL质量分数为98%的H2SO4,用水稀释至100 mL,H2SO4的 质量分数为9.8% |
| B、在H2O2+Cl2═2HCl+O2反应中,每生成32 g氧气,则转移2NA个电子 |
| C、标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4 L,质量为28 g |
| D、一定温度下,1 L 0.50 mol/L NH4Cl溶液与2 L 0.25 mol/L NH4Cl溶液含NH4+的物质的量相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com