
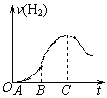 某化学研究性小组在用铝与稀硫酸的反应制氢气的实验时发现,如果把在空气中放置一段时间的5.0 g铝片放入圆底烧瓶中,然后通过分液漏斗加入500 mL 0.5 mol/L硫酸溶液,充分反应后,该小组同学根据记录数据得到了产生氢气的速率与反应时间的关系图象(如右图所示) ,请你帮助该小组同学回答下列问题 :
某化学研究性小组在用铝与稀硫酸的反应制氢气的实验时发现,如果把在空气中放置一段时间的5.0 g铝片放入圆底烧瓶中,然后通过分液漏斗加入500 mL 0.5 mol/L硫酸溶液,充分反应后,该小组同学根据记录数据得到了产生氢气的速率与反应时间的关系图象(如右图所示) ,请你帮助该小组同学回答下列问题 :
(1)曲线OA段不产生氢气的原因是_____________ _ ______
____________________ _____,
有关的离子反应方程式为_________________________ _____ _____
(2)曲线BC段产生氢气的速率突然加快的主要原因是
____________________________________________________________________________
(3)点C以后产生氢气的速率逐渐减小的主要原因是
____________________________________________________________________________
(4)从理论上分析该小组同学能收集到氢气的体积为(标准状况下)___________
 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
已知A、B、C、D、E是短周期的五种元素,它们的原子序数依次增大。通常A元素原子形成的离子核外电子数为零;C、D、E三种元素的最高价氧化物对应水化物之间可以两两反应;A与C同主族;B与E同主族;E的单质为黄色晶体,易溶于二硫化碳。
(1)写出B元素的名称: 。
(2)A与C能形成离子化合物CA,试画出其中阴离子的结构示意图 ;
(3)A、B、C三种元素形成的化合物所含的化学键类型为 。
(4)B、D、E三种元素的离子半径由大到小的顺序为 (用离子符号表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
蛇纹石由MgO、A12O3、SiO2、Fe2O3 组成。现取一份蛇纹石试样进行实验,首先将其溶 于过量的盐酸,过滤后,在所得的沉淀X和溶液Y中分别加入NaOH溶液至过量。下列叙述不正确的是
A.沉淀X的成分是SiO2
B.将蛇纹石试样直接溶于过量的NaOH溶液后过滤,可得到红色颜料Fe2O3
C.在溶液Y中加入过量的NaOH溶液,过滤得到的沉淀的主要成分是Fe(OH)3 和Mg(OH)2
D.溶液Y中的阳离子主要是Mg2+、Al3+、Fe3+、H+
查看答案和解析>>
科目:高中化学 来源: 题型:
在反应C(s)+CO2(g)=2CO(g)中,能使反应速率加快的是
①增大压强 ②升高温度 ③将C粉碎 ④通CO2气体 ⑤加入足量木炭粉
A.①②③ B. ①②④ C. ①②③④ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
用铝粉和氧化铁粉末配成的铝热剂,分成两等份:一份在高温下恰好完全反应,再与足量稀硫酸反应,生成氢气aL;另一份直接放入足量烧碱溶液中充分反应,在相同条件下生气氢气bL,则体积比a:b为
A.1:1 B.3:2 C.2:3 D.1:4
查看答案和解析>>
科目:高中化学 来源: 题型:
室温下,下列溶液中粒子浓度大小关系正确的是
A.Na2S溶液:c(Na+)>c(HS-)>c(OH-)>c(H2S)
B.Na2C2O4溶液中:c(OH-)=c(H+)+c(HC2O4-)+2c(H2C2O4)
C.Na2CO3溶液:c(Na+)+c(H+)=2c(CO32-)+c(OH-)
D.CH3COONa和CaCl2混合溶液:c(Na+)+c(Ca2+)=c(CH3COO-)+c(CH3COOH)+2c(Cl-)
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
A.常温常压下,16 g O3气体含有氧原子数为NA
B.标准况状下,44.8 L四氯化碳含有的分子数为2NA
C.0.1 mol·L-1氯化铝溶液中含有Al3+数为0.1NA
D.2.4 g金属镁变为镁离子时失去的电子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
叠氮化钠(NaN3)是汽车安全气囊中的主要成分,能在发生碰撞的瞬间分解产生大量气体将气囊鼓起。实验室测定叠氮化钠样品中NaN3的质量分数。实验步骤如下:
①称取2.5000 g叠氮化钠试样,配成250 mL溶液。
②准确量取25.00 mL溶液置于锥形瓶中,用滴定管加入50.00 mL 0.1000 mol·L-1(NH4)2Ce(NO3)6(六硝酸铈铵)[发生反应为2(NH4)2Ce(NO3)6+2NaN3===4NH4NO3+2Ce(NO3)3+2NaNO3+3N2↑](杂质不参与反应)。
③反应后将溶液稍稀释,然后向溶液中加入5 mL浓硫酸,滴入2滴邻菲罗啉指示液,用0.0500 mol·L-1(NH4)2Fe(SO4)2(硫酸亚铁铵)标准滴定溶液滴定过量的Ce4+至溶液由淡绿色变为黄红色(发生的反应为:Ce4++Fe2+===Ce3++Fe3+),消耗硫酸亚铁铵标准溶液24.00 mL。
(1)步骤①配制叠氮化钠溶液时,除需用到烧杯、玻璃棒、量筒外,还用到的玻璃仪器有________、________。
(2)叠氮化钠受撞击时生成两种单质,反应的化学方程式为____。
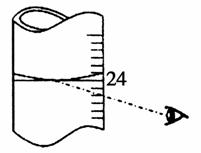
(3)若其他读数正确,滴定到终点后,读取滴定管中(NH4)2Fe(SO4)2标准溶液体积,按如图图示读取,将导致所测定样品中叠氮化钠质量分数________(选填:“偏大”、“偏小”或“不变”)
(4)通过计算确定叠氮化钠试样中含NaN3的质量分数为多少(写出计算过程)?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com