
 ④CH≡CH ⑤NH3 ⑥CH4
④CH≡CH ⑤NH3 ⑥CH4| A.①②③ | B.①⑤⑥ | C.②③④ | D.③⑤⑥ |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
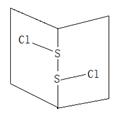
| A.为非极性分子 |
| B.分子中既含有极性键又含有非极性键 |
| C.与S2Br2结构相似,熔沸点S2Br2>S2Cl2 |
| D.与水反应的化学方程式可能为2S2Cl2+2H2O= SO2↑+3S↓+4HCl |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.不是所有的共价键(σ 键)都具有方向性 |
| B.N≡N键能大于C≡C的键能,所以N≡N不易发生加成反应 |
| C.根据价层电子对互斥理论可知,OF2分子的极性小于H2O分子的极性 |
| D.Na原子基态核外电子占有3个能层,4种能级,6个原子轨道。有6种电子运动状态 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.活化分子之间的碰撞一定是有效碰撞 |
| B.升高温度时,活化分子百分数增加 |
| C.反应物分子的每次碰撞都能发生化学反应 |
| D.有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.C3O2可以在氧气中完全燃烧生成CO2 |
| B.C3O2和CO2都是碳的氧化物,它们互为同分异构体 |
| C.COS是由极性键构成的非极性分子,分子中所有原子都满足8电子稳定结构 |
| D.COS在氧气中完全燃烧后,生成物是CO2和SO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com