
在3种不同条件下,分别向容积为2 L的恒容密闭容器中充入2 mol A和1 mol B,发生反应如下:2A(g)+B(g)2D(g)
ΔH=-Q kJ·mol-1。相关条件和数据见下表:
| 实验编号 | 实验Ⅰ | 实验Ⅱ | 实验Ⅲ |
| 反应温度/℃ | 800 | 800 | 850 |
| 达平衡时间/min | 40 | 10 | 30 |
| c(D)平衡/mol·L-1 | 0.5 | 0.5 | 0.15 |
| 反应的能量变化/kJ | Q1 | Q2 | Q3 |
下列说法正确的是( )
A.可用压强或密度是否发生变化判断上述反应是否达到平衡
B.实验Ⅱ可能隐含的条件是使用催化剂,实验Ⅲ达平衡时v(D)为0.005 mol·L-1·min-1
C.由表中信息可知Q>0,并有Q3<Q2=Q1=Q
D.实验Ⅰ达平衡后,恒温下再向容器中通入1 mol A和1 mol D,达平衡时c(D)为1.0 mol·L-1
答案 BD
解析 A项,不能用密度不变判断上述反应是否达到平衡;B项,Ⅰ 和 Ⅱ 达到平衡时,c(D)相等,隐含的条件是使用催化剂,实验Ⅲ达到平衡时v(D)= =0.005 mol·L-1·min-1;C项,升温 c(D)减小,平衡左移,Q>0,Q3<Q2=Q1<Q;
=0.005 mol·L-1·min-1;C项,升温 c(D)减小,平衡左移,Q>0,Q3<Q2=Q1<Q;
D项, 2A(g) + B(g)2D(g)
原平衡(mol·L-1) 0.5 0.25 0.5
K=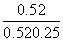 =4
=4
当再加入0.5 mol·L-1的A和0.5 mol·L-1的D时
c(A)=1 mol·L-1
c(B)=0.25 mol·L-1
c(D)=1 mol·L-1
此时Q=4, 平衡不移动,所以c(D)为1.0 mol·L-1。


科目:高中化学 来源: 题型:
下列各组元素,按原子半径依次减小,元素第一电离能逐渐增大的顺序排列的是( )
A.K、Na、Li B.Al、Mg、Na C.N、O、C D.Cl、S、P
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如下表:
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | 常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为34 |
(用推断出的元素符号回答问题)
(1)Z位于元素周期表第 周期第 族,Y的氢化物电子式是 。
(2)XY2是一种常用的溶剂,XY2的分子中存在 个σ键。在H—Y、H—Z两种共价键中,键的极性较强的是 ,键长较长的是 ,对应氢化物较稳定的是 。
(3)写出X的单质与Y的最高价氧化物对应水化物的浓溶液反应的方程式 。
(4)写出W元素的原子核外价电子排布式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
高炉炼铁过程中发生的反应: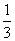 Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g)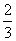 Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下表所示,下列说法不正确的是( )
Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下表所示,下列说法不正确的是( )
| 温度/℃ | 1 000 | 1 150 | 1 300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
A.ΔH<0
B.该反应的平衡常数表达式是K=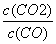
C.其他条件不变,向平衡体系充入CO2气体,K值减小
D.其他条件不变,升高温度,可以降低CO的平衡转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
下图为直流电源电解稀Na2SO4水溶液的装置。通电后在石墨电极a和b附近分别滴加几滴石蕊溶液。下列实验现象描述正确的是( )
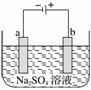
A.逸出气体的体积,a电极的小于b电极的
B.一电极逸出无味气体,另一电极逸出刺激性气体
C.a电极附近呈红色,b电极附近呈蓝色
D.a电极附近呈蓝色,b电极附近呈红色
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上用电解法处理含镍酸性废水并得到单质Ni的原理如图所示。
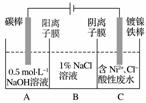
下列说法不正确的是( )
已知:①Ni2+在弱酸性溶液中发生水解
②氧化性:Ni2+(高浓度)>H+>Ni2+(低浓度)
A.碳棒上发生的电极反应:4OH--4e-===O2↑+2H2O
B.电解过程中,B中NaCl溶液的物质的量浓度将不断减少
C.为了提高Ni的产率,电解过程中需要控制废水pH
D.若将图中阳离子膜去掉,将A、B两室合并,则电解反应总方程式发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)[2014·四川理综,11(4)]MnO2可作超级电容器材料。用惰性电极电解MnSO4溶液可制得MnO2,其阳极的电极反应式是__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com