
| A. | 一氧化碳极易与血红蛋白结合,所以有毒 | |
| B. | 氧气易溶于水,所以鱼能生存 | |
| C. | 金刚石和石墨都是碳元素组成的单质,所以性质相似 | |
| D. | 溶液由溶质和溶剂组成,所以溶液体积等于溶质体积加溶剂体积 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 7.8g N2O2晶体中阴离子数目为0.2NA | |
| B. | 含1mol NH4Cl和少量NH3•H2O的中性溶液中,NH${\;}_{4}^{+}$数目为NA | |
| C. | 电解精炼铜时,阳极质量减少64g外电路导线上通过的e-数目为NA | |
| D. | 室温下,1L pH=13的NaOH溶液中,由水电离的OH-数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
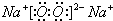 ;B的氢化物的结构式为
;B的氢化物的结构式为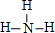 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 离子晶体 | 原子晶体 | 分子晶体 |
| A | NaOH | Ar | SO2 |
| B | H2SO4 | 石墨 | S |
| C | CH3COONa | 水晶 | 苯 |
| D | Ba(OH)2 | 金刚石 | 玻璃 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
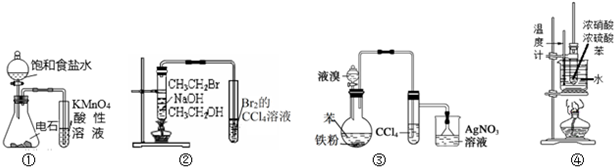
| A. | 装置①可用于检验乙炔的还原性 | |
| B. | 装置②可以证明CH3CH2Br发生消去反应生成了乙烯 | |
| C. | 装置③可以证明苯生成溴苯的反应是取代反应 | |
| D. | 装置④可用于实验室制备硝基苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
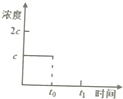 请你利用所学反应原理知识解决下列问题:
请你利用所学反应原理知识解决下列问题:| 酸 | 电离方程式 | 电离平衡常数K |
| CH3COOH | CH3COOH?CH3COO-+H+ | 1.96×10-5 |
| HClO | HClO?ClO-+H+ | 3.0×10-8 |
| H2CO3 | H2CO3?H++HCO3- HCO3-?H++CO32- | K1=4.4×10-7 K2=5.6×10-11 |
| H3PO4 | H3PO4?H++H2PO4- H2PO4-?H++HPO42- HPO42-?H++PO43- | K1=7.1×10-3 K2=6.3×10-8 K3=4.2×10-13 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

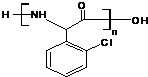 ;D→E所需X物质的结构简式:
;D→E所需X物质的结构简式:
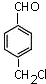 .
.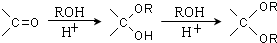
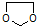 的合成路线流程图(无机试剂任选).合成路线流程图示例如下:
的合成路线流程图(无机试剂任选).合成路线流程图示例如下:
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
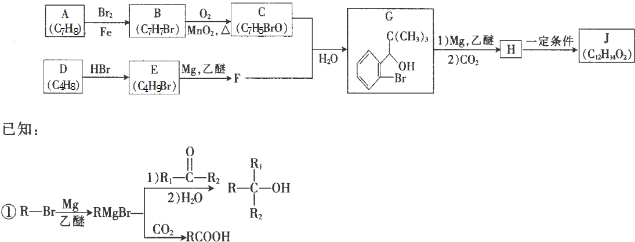
 .
.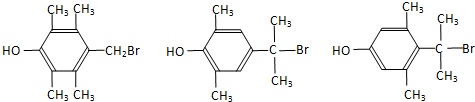 (写出一种即可).
(写出一种即可).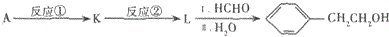
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它与金刚石互为同素异形体 | |
| B. | 它与C60互称同分异构体 | |
| C. | 它与C60的物理性质与化学性质完全相同 | |
| D. | 它与13C互为同位素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com