
【题目】已知几种难溶电解质的溶度积如下表所示:
几种难溶电解质的Ksp(25℃) | |
沉淀溶解平衡 | Ksp |
AgBr(s) | 5,0×10-13 mol2·L-2 |
AgI(s) | 8.3×10-17 mol2·L-2 |
FeS(s) | 6.3×10-18 mol2·L-2 |
ZnS(s) | 1.6×10-24 mol2·L-2 |
CuS(s) | 1.3×10-36 mol2·L-2 |
(1)AgBr、AgI、FeS、ZnS、CuS的溶解能力由大到小的顺为:____________________。
(2)向饱和的AgI溶液中加入固体硝酸银,则c( I- )________(填“增大”、“减小”或“不变”),若改加AgBr固体,则c(Ag+)__________(填“增大”、“减小”或“不变”)。
(3)在25℃时,向100mL浓度均为0.1 mol·L-1 FeCl2、ZnCl2、CuCl2的混合溶液中逐滴加入Na2S溶液,生成的沉淀的先后顺序是_____________________(用沉淀物的化学式表示)。
(4)在25℃时,把ZnS加入蒸馏水中,一定时间后达到如下平衡: ZnS(s)![]() Zn2+(aq)+S2-(aq),下列措施可使ZnS减少的是 _______。
Zn2+(aq)+S2-(aq),下列措施可使ZnS减少的是 _______。
A.加入少量CuS固体 B.加入少量FeS固体
C.加入少量FeCl2固体 D.加入少量CuCl2固体
【答案】 AgBr>AgI>FeS>ZnS>CuS 减少 增大 CuS ZnS FeS CD
【解析】试题分析:(1)AgBr、AgI、FeS、ZnS、CuS结构相似,溶度积越大,溶解能力越强,AgBr>AgI>FeS>ZnS>CuS;(2)碘化银的溶度积不变,加入硝酸银,银离子浓度增大,所以[I-]减小;AgBr的溶度积大于碘化银的溶度积,所以加入AgBr,[Ag+]增大;(3)最先生成溶度积小的物质,生成的沉淀的先后顺序是CuS、ZnS、FeS;(4)ZnS 的溶度积大于CuS,故A错误;ZnS 的溶度积小于FeS,FeS 能转化为ZuS,故B错误;加入少量FeCl2固体,生成FeS,ZnS减少,故C正确;加入少量CuCl2固体,生成CuS,ZnS减少,故D正确;


科目:高中化学 来源: 题型:
【题目】下列各组离子,能在水溶液中大量共存的是
A. K+、SO42-、HCO3-、H+ B. NH4+、Cl-、OH-、Na+
C. CO32-、Na+、K+、OH- D. Na+、Ag+、H+、I-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水溶液中能大量共存的一组离子是( )
A.NH4+、Ba2+、Br﹣、CO32﹣
B.Cl﹣、SO32﹣、Fe2+、H+
C.K+、Na+、SO42﹣、MnO4﹣
D.Na+、H+、NO3﹣、HCO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数,下列说法正确的是 ( )
A. 2.4g金属镁所含电子数目为0.2NA B. 16g CH4所含原子数目为NA
C. 17gNH3所含质子数目为10 NA D. 18g水所含分子数目为18NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】括号内物质为杂质,在实验室中,下列除杂的方法中正确的是
A.溴苯(溴):加入KI溶液,振荡,分液
B.乙烷(乙烯):通入H2在一定条件下反应,使乙烯转化为乙烷
C.乙醇(水):用生石灰吸水后蒸馏
D.乙烯(CO2和SO2):将其通入酸性KMnO4溶液中洗气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己二酸是一种重要的化工原料和合成中间体。已知:室温下,己二酸微溶于水,当温度由28℃升至78℃时,其溶解度可增大20倍。某实验小组利用绿色氧化剂H2O2氧化环己烯合成己二酸,反应和制备装置如下:

主要实验步骤:
①在100mL三颈烧瓶中依次加入1.50g钨酸钠0.57g草酸和34mL30%过氧化氢溶液,室温下磁力搅拌20min。
②用恒压滴液漏斗缓慢加入8.0mL的环己烯,继续搅拌并加热回流2小时,停止加热。
③将反应液迅速转入烧杯中,冷却至室温后再用冰水浴冷却,有大量晶体析出。抽滤,并用少量冰水洗涤,即可得到己二酸晶体粗品。
回答下列问题:
(1)本实验中使用带刻度的恒压滴液漏斗的主要作用有_________、_________。
(2)步骤③中用冰水洗涤晶体的目的是______________________________________。
己二酸晶体粗品可利用_________方法进一步获得纯品。
(3)取0.1480g己二酸(Mr=146.0)样品置于250mL锥形瓶中,加入50mL蒸馏水溶解,再加入2滴指示剂,用0.1000mol/Ld的NaOH标准溶液滴定至终点,消耗NaOH溶液的体积为20.00mL。
①本实验应选择_________(填“甲基橙”“石蕊”或“酚酞”)溶液作指示剂。
②判断滴定终点的方法是_________________________。
③样品中己二酸的质量分数为_________%(保留4位有效数字)。
(4)实验小组通过改变环己烯的用量来探究物料比对产率的影响,实验结果如下图所示。

结合图像分析产率变化的可能原因:
①A点→B点:___________________________________________;
②B点→C点:____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年,美国研究小组开发出一种以糖为能源,可循环使用的环保电池装置。其工作原理如图所示。下列说法错误的是
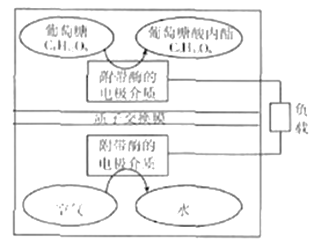
A. 葡萄糖在电池负极发生反应
B. 装置所示原理可以在强碱性条件下进行
C. 装置正极电极反应式为:O2+4e-+4H+=2H2O
D. 装置工作时,每消耗180g葡萄糖,将有2mol质子通过交换膜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的化合物应用广泛,但氮氧化物也是主要的空气污染物之一,要对其进行处理和再利用。
I.脱硝法:
(1)已知H2的燃烧热△H= -285.8kJ/mol,N2(g) +O2(g)=2NO(g) △H= + 180kJ/mol。一定条件下,H2还原NO生成液态水和一种无毒物质的热化学方程式为_______________________。
II.化合法:
工业上用NO和Cl2化合制备重要的合成用试剂NOCl( 亚硝酰氯)气体。
(2)NOCl中N 元素的化合价为__________,NOCl的电子式为_____________________。
(3)向1L恒容密团容器中通入2molNO(g)和1molCl2(g)发生反应:2NO(g) + Cl2(g)![]() 2NOCl(g) △H,在不同温度下测得c(NOCl)与时间t的关系如图所示。
2NOCl(g) △H,在不同温度下测得c(NOCl)与时间t的关系如图所示。
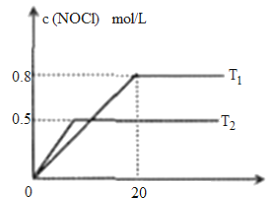
①该反应的△H_____0(填“>"或“<”或“=”),理由是_____________________。
②温度T1时,Cl2(g)在0~20min的平均反应速率为__________mol/(L·min)。
③温度T2时,该反应的平衡常数K=______(结果保留小数点后2位)。若反应在T2达到平衡后,再向容器中充入2molNO(g)和1molCl2(g),当再达平衡时,c(NOCl)=______(填“>”或“<”或“一”)1mol/L。
III.电化学法:
用下图所示装置可以模拟消除NO2获得铵态氮肥的过程。
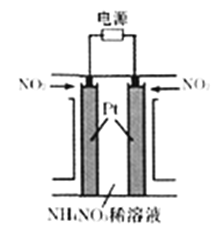
(4)该装置阳极电极反应式为____________________________。
(5)电解后,向所得溶液中通入适量NH3可增加铵态氮肥的产量,理由是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸锰在锰系产品中具有重要地位,由软锰矿(MnO2) 和硫铁矿(FeS2)制备流程如下:
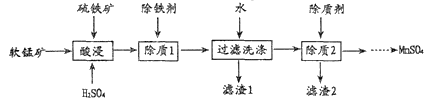
(1)从“除质2”后的溶液中得到MnSO4的操作为______、降温结晶、过滤和干燥。
(2)下图是在一定条件下,不同浓度的硫酸对各元素浸出率的影响,由此得出的相关结论是:

①__________;②__________。提高软锰矿浸出率的措施还有______和_______。
(3)除铁剂为H2SO5和氨水。
①H2SO5 中S的化合价为+6,其中过氧键的数目为______,加入其目的是_________。
②写出Fe3+生成沉淀黄铵铁矾NH4Fe3(SO4)2(OH)6的离子方程式____________。
(4)工业除质剂为MnF2,发生反应为(已知,该温度下MnF2、CaF2 和MgF2 的Ksp分别为5.0×10-3、2.0×10-10、8.0×10-11)
反应I:MnF2(s) +Ca2+=CaF2(s) +Mn2+
反应II:MnF2(s) +Mg2+=MgF2(s) + Mn2+
若滤液中c(Mg2+) =0.02 mol/L,加入MnF2(s),使Ca2+恰好沉淀完全即溶液中c(Ca2+) =1.0×10-5mol/L,此时是否有MgF2 沉淀生成?_________(列式计算)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com