
| A、I2O4 |
| B、I3O5 |
| C、I4O7 |
| D、I4O9 |
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:高中化学 来源: 题型:
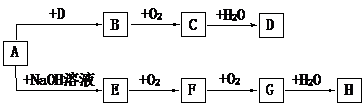
查看答案和解析>>
科目:高中化学 来源: 题型:
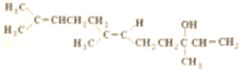
| A、能使酸性KMnO4溶液褪色 |
| B、既能发生取代反应,也能发生加成反应 |
| C、1mol橙花醇在室温下与修的四氯化碳溶液反应,最多消耗240gBr2 |
| D、1mol橙花醇在氧气中充分燃烧,需消耗470.4L氧气(标准状况) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、水的离子积仅适用于纯水 |
| B、水的电离和电解都需要电 |
| C、升高温度一定使水的离子积增大 |
| D、加入电解质一定会破坏水的电离平衡 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、二氧化硅分子的结构式:O=Si=O | ||
B、CO2分子比例模型: | ||
C、H2O2的电子式: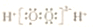 | ||
D、质子数为8,中子数为10的氧原子:
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、4 mol?L-1 H2SO4 |
| B、改用含0.1 mol 的98%的浓硫酸 |
| C、硫酸镁 |
| D、硫酸铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com